
(1)250C、101kPa时,____________纯物质完全燃烧生成稳定的化合物时所放出的热量,叫做该物质的燃烧热。
(2)某温度下,纯水中的c(H+)=2.0×10-7mol/L,则此时溶液的c(OH-)为 ;
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
 已知在25℃、1.013×105Pa下,1mol氢气完全燃烧生成液态水放出285kJ的热量,请回答下列问题:
已知在25℃、1.013×105Pa下,1mol氢气完全燃烧生成液态水放出285kJ的热量,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、水是一种非电解质 | B、纯水中c(H+)随着温度的升高而降低 | C、250C时,pH相同的NaOH溶液与醋酸钠溶液,水的电离度前者小于后者 | D、由液态水结成冰的过程是一个熵增的过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(5分)已知AgCl为难溶于水和酸的白色固体,Ag2S为难溶于水和酸的黑色固体。向AgCl和水的悬浊液中加入足量的Na2S溶液并振荡,结果白色固体完全转化为黑色固体:(250C时AgCl,Ag2S的溶解度分别为1.5 ×10-4g, 1.3 × 10-16g)
(1)写出白色固体转化成黑色固体的化学方程式:
(2)白色固体转化成黑色固体的原因是:
查看答案和解析>>
科目:高中化学 来源:2012-2013学年湖北省黄冈市高三上学期期末考试理综化学试卷(解析版) 题型:填空题
煤的气化是高效、清洁地利用煤炭的重要途径之一。
(1)在250C 101kPa时,H2与O2化合生成1mol H2O(g)放出241.8kJ的热量,其热化学方程式为
___________
又知: ①C(s)+O2(g)═CO2(g) △H=-393.5kJ/mol
②CO(g)+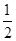 O2(g)═CO2(g) △H=-283.0kJ/mol
O2(g)═CO2(g) △H=-283.0kJ/mol
焦炭与水蒸气反应是将固体煤变为气体燃料的方法,C(s)+H2O(g)═CO(g)+H2(g) △H=____kJ/mol
(2) CO可以与H2O(g)进一步发生反应: CO(g)+H2O(g)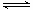 CO2(g)+H2(g) △H<0在恒容密闭容器中,起始时n(H2O)=0.20mol,n(CO)=0.10 mol,在8000C时达到平衡状态,K=1.0,则平衡时,容器中CO的转化率是_____________(计算结果保留一位小数)。
CO2(g)+H2(g) △H<0在恒容密闭容器中,起始时n(H2O)=0.20mol,n(CO)=0.10 mol,在8000C时达到平衡状态,K=1.0,则平衡时,容器中CO的转化率是_____________(计算结果保留一位小数)。
(3) 工业上从煤气化后的混合物中分离出H2,进行氨的合成,已知反应反应N2(g)+3H2(g 2NH3(g)(△H<0)在等容条件下进行,改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示:
2NH3(g)(△H<0)在等容条件下进行,改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示:

①N2的平均反应速率v1(N2)、vII(N2)、vIII(N2)从大到小排列次序为________;
②由第一次平衡到第二次平衡,平衡移动的方向 是________,采取的措施是________。
③比较第II阶段反应温度(T2)和第III阶段反应速度(T3)的高低:T2________T3填“〉、=、<”判断的理由是________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com