
| A. | NaOH | B. | K2CO3 | C. | Na2O | D. | H2SO4 |
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:解答题
| 实验方案 | 实验现象 |
| ①将镁带用砂纸擦后,放入试管中,加入少量水后,加热至水沸腾;再向反应后溶液中滴加酚酞 | (A)浮于水面,熔成一个小球,四处游动,发出“嘶嘶”声,随之消失,溶液变红色 |
| ②将一小块金属钠放入滴有酚酞试液的冷水反应 | (B)反应不十分剧烈,产生的气体可在空气中燃烧 |
| ③镁带与2mol/L的稀盐酸反应 | (C)剧烈反应,产生的气体可在空气中燃烧 |
| ④铝条与2mol/L的稀盐酸反应 | (D)生成白色胶状沉淀,继而沉淀消失 |
| ⑤向AlCl3溶液滴加NaOH溶液 | (E)产生大量气体,可在空气中燃烧,溶液变红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 实验操作 | 现象 |
① | 向大试管中加入20mL 0.1mol?L-1的Na2S溶液 (已知Na2S溶液显碱性,pH约为12),再滴加5mL 0.1mol?L-1的FeCl3溶液,边滴边振荡 | 产生大量黑色沉淀,反应后溶液仍显碱性 |
② | 向另一支大试管中加入20mL 0.1mol?L-1FeCl3溶液(已知FeCl3溶液显酸性,pH约为2),再滴加5mL 0.1mol?L-1的Na2S溶液,边滴边振荡 | 局部有黑色沉淀但瞬间消失,溶液颜色变浅,并产生大量黄色浑浊,反应后溶液仍显酸性 |
| 实验操作 | 预期现象和结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


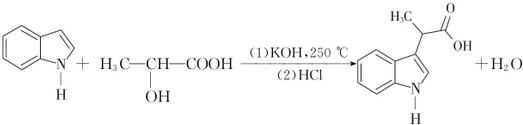
 .
. .
. (填结构简式).
(填结构简式). 经如下步骤合成:
经如下步骤合成:
 的反应类型为还原反应,反应条件2为催化剂、加热,其反应的化学方程式为
的反应类型为还原反应,反应条件2为催化剂、加热,其反应的化学方程式为 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3+ (Al3+),加过量的氨水,过滤 | |
| B. | KCl溶液(BaCl2),加入足量的K2SO4溶液,过滤 | |
| C. | CO2 (SO2),将混合气体通过依次饱和碳酸氢钠溶液和浓硫酸,洗气 | |
| D. | NaHCO3溶液(Na2CO3溶液):加入适量的Ca(OH)2溶液,过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;②中离子方程式为Br-+Ag+═AgBr↓;
;②中离子方程式为Br-+Ag+═AgBr↓; 、Br2,要想得到纯净的产物,可用NaOH溶液(或水)试剂洗涤,洗涤后分离粗产品应使用的仪器是分液漏斗;
、Br2,要想得到纯净的产物,可用NaOH溶液(或水)试剂洗涤,洗涤后分离粗产品应使用的仪器是分液漏斗; ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无法确定 | B. | 0.2mol | C. | 0.4mol | D. | 0.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在有机物A分子中,具有酚羟基、醇羟基、羧基等官能团,其结构简式如图.
在有机物A分子中,具有酚羟基、醇羟基、羧基等官能团,其结构简式如图. ;
; ;
; ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使酚酞变红色的溶液中:Na+、Al3+、SO42-、Cl- | |
| B. | 能使KSCN试液变红的溶液中:H+、Zn2+、SO32-、SO42- | |
| C. | 与Al反应能放出H2的溶液中:Fe2+、K+、NO3-、SO42- | |
| D. | 显强碱性的溶液中:K+、Na+、AlO2-、CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com