
����Ŀ����֪����K2Cr2O7��Һ����FeSO4��Ӧ����Fe3+��Cr3+���ֽ������ữ��K2Cr2O7��Һ��FeSO4��Һ��ϣ���ַ�Ӧ������������Һ�м���KI��Һ�������Һ��Fe3+�����ʵ���������KI�����ʵ����ı仯��ϵ ��ͼ��ʾ������˵���в���ȷ������ ��

A.ͼ��AB�ε�������ΪK2Cr2O7
B.ͼ��BC�η����ķ�ӦΪ2Fe3++2I-=2Fe2++I2
C.��ʼ�����K2Cr2O7Ϊ0.25 mol
D.K2Cr2O7��FeSO4��ʼ��Ӧʱ���ʵ���֮��Ϊ1��3
���𰸡�D
��������
���������A����ʼʱFe3+Ũ�Ȳ��䣬��˵��Fe3+û�вμӷ�Ӧ����ABӦΪK2Cr2O7�͵⻯�صķ�Ӧ��K2Cr2O7Ϊ����������A��ȷ��B��BC��Fe3+Ũ����С��Ϊ�����Ӻ͵⻯�صķ�Ӧ����Ӧ�����ӷ���ʽΪ2Fe3++2I-=2Fe2++I2����B��ȷ��C�����������ͻ�ԭ����ʧ������Ŀ��ȿ�֪��Ӧ�Ĺ�ϵʽΪK2Cr2O7��6Fe3+��6I-�������ĵ�n��I-��=1.5mol����ʼ�����K2Cr2O7�����ʵ���Ϊ![]() mol=0.25mol����C��ȷ��D���ɷ���ʽ2Fe3++2I-��2Fe2++I2��֪��BC������KI0.9mol����n��Fe3+��=n��Fe2+��=0.9mol��K2Cr2O7����FeSO4��Ӧ�����ʵ���Ϊ0.25mol��0.9mol=5��18����D������ѡD��
mol=0.25mol����C��ȷ��D���ɷ���ʽ2Fe3++2I-��2Fe2++I2��֪��BC������KI0.9mol����n��Fe3+��=n��Fe2+��=0.9mol��K2Cr2O7����FeSO4��Ӧ�����ʵ���Ϊ0.25mol��0.9mol=5��18����D������ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�����Ͽ�������C��ͨ�����з�Ӧ�ϳɣ�

�����й�������ȷ������ ��
A������A������̼ԭ���п���λ��ͬһƽ��
B������B����4molH2�����ӳɷ�Ӧ
C��������KMnO4��Һ����������C���Ƿ���CH3��CH2��17OH
D��B����C�ķ�Ӧ����Ϊȡ����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ֿ���������A��B��C��D��E���������������������ӻ�����ͬ���ֱ�������������K+��Fe3+��Cu2+��Ba2+��Al3+������������Cl����OH����NO3����CO32����X�е�һ�֡�
��1��ijͬѧͨ���ȽϷ�������Ϊ�������Ϳ��ж����б��е�����������_________��_________��
��2������C�к�������X��Ϊ��ȷ��X���ֽ���1���е��������ʼ�ΪA��B����C��A����Һ���ʱ��������ɫ��������ó����е���ϡHNO3�����������ܽ⣬ʣ���ɫ���壬��XΪ ������ţ���
A��Br�� B��SO42�� C��CH3COO�� D��HCO3��
��3����19.2gCuͶ��װ������D��Һ���Թ��У�Cu���ܽ⣬�ٵμ�ϡH2SO4��Cu���ܽ⣬�ܿڸ����к���ɫ������֣�д��Cu�ܽ�����ӷ���ʽ ��
��Ҫ��Cu��ȫ�ܽ⣬���ټ���H2SO4�����ʵ����� ��
��4��E��Һ������ᷴӦʱ��������ɫ���ʣ��÷�Ӧ�����ӷ���ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ���ܽ�Al��OH��3�������ܽ�SiO2���ڸ���Һ�п��Դ����������������
A��Fe2+��Na+��Cl����NO3�� B��Fe3+��Ca2+��CH3COO����HCO3��
C��Na+��Mg2+��NO3����SO42�� D��Na+��K+��Cl����[Al(OH)4]��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��MnO2��һ����Ҫ�������ܲ��ϣ���MnO2���ᴿ�ǹ�ҵ��������Ҫ���ڡ�ij�о���ѧϰС������˽���MnO2�����н϶��MnO��MnCO3����Ʒת��Ϊ��MnO2��ʵ�飬���������£�

��1����������ϡH2SO4ʱ����MnO2��Ʒ�е� ��д��ѧʽ��ת��Ϊ���������ʣ�д������CO2��һ���Ļ�ѧ����ʽ ��
��2����������Ӧ�����ӷ���ʽ�� ��
��3�������������������������������̨������Ȧ�����ƾ��ơ��������� ����֪�����õ��Ĺ�������NaClO3��NaOH����һ�������� ��д��ѧʽ����
��4������MnO2��Ʒ������Ϊ12.69g����������Ӧ�����˵õ�8.7g MnO2�����ռ���0.224L CO2����״���£������ڵ�������Ӧ��������Ҫ mol NaClO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ŀǰ����������������Ⱦ�ж��ַ�����
��1����CH4����ԭ��������������������������Ⱦ����֪��
��CH4 ��g��+4NO2 ��g����4NO��g��+CO2 ��g��+2H2 O��g�� ��H����574 kJ��mol��1
��CH4 ��g��+4NO��g����2N2 ��g��+CO2 ��g��+2H2 O��g�� ��H����1160 kJ��mol��1
��H2O��g����H2O��l�� ��H����44��0 kJ��mol��1
д��CH4��g����NO2��g����Ӧ����N2��g����CO2��g����H2O��l�����Ȼ�ѧ����ʽ________
��2���û���̿��ԭ��������������йط�ӦΪ��C��s��+2NO��g�� ![]() N2 ��g��+CO2 ��g��ij�о�С��������ܱ���������һ�����Ļ���̿NO�����������·�Ӧ����Ӧ���е���ͬʱ���ø����ʵ�Ũ������
N2 ��g��+CO2 ��g��ij�о�С��������ܱ���������һ�����Ļ���̿NO�����������·�Ӧ����Ӧ���е���ͬʱ���ø����ʵ�Ũ������
Ũ��/mol��L-1 ʱ��/min | NO | N2 | CO2 |
0 | 0.100 | 0 | 0 |
10 | 0.058 | 0.021 | 0.021 |
20 | 0.040 | 0.030 | 0.030 |
30 | 0.040 | 0.030 | 0.030 |
40 | 0.032 | 0.034 | 0.017 |
50 | 0.032 | 0.034 | 0.017 |
��������Ϊ�жϷ�Ӧ�ﵽ��ѧƽ��״̬��������_____ __
A��������CO2��Ũ�ȱ��ֲ���
B��v����N2��=2 v����NO��
C��������ѹǿ���ֲ���
D�����������ܶȱ��ֲ���
E����������ƽ����Է����������ֲ���
���ڸ��¶���ʱ���÷�Ӧ��ƽ�ⳣ��Ϊ ��������λС������
����30 min���ı�ijһ��������Ӧ���´ﵽƽ������ı��������___ __��
��3���ϳ���ʧȥ���Եĸ�п��ý�������Ʊ�п�̵�ء��ڼ��������£��õ�ص��ܷ�ӦΪ��Zn��s��+2MnO2 ��s��+H2O��l��= Zn��OH��2 ��s��+Mn2O3��s�����õ�������ĵ缫��Ӧʽ�� ��PbO2 ����ͨ��ʯīΪ�缫��Pb��NO3��2��Cu��NO3��2�Ļ����ҺΪ���Һ�����ȡ������������Ӧ�ĵ缫��ӦʽΪ �������Ϲ۲쵽�������� �������Һ�в�����Cu��NO3��2����������Ҫȱ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ŀǰ�ƹ�ʹ�õ���ˮΪ�ܼ��ķ����-ˮ��������������ܽ�O2�����½������������ߣ�Ϊ��Ҫ��ˮ�����м��뻺ʴ�������¿���Ϊ��ʴ�����ӵ��� �� ��
A��KMnO4 B��NaNO2 C��FeCl3 D��HNO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����۸����ȶ�, ���ױ����������������Ǹ�ˮ����{ [Cr(CH3COO)2]2��2H2O����Է�������Ϊ376����һ�����ɫ���壬��������ˮ���ѣ����������ᣬ�dz��õ��������ռ���ʵ��������п����CrCl3��Һ����������Һ������Ϊ��Ҫԭ���Ʊ������Ǹ�ˮ�����װ������ͼ��ʾ��
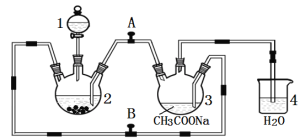
�Ʊ������з����ķ�Ӧ���£�
Zn(s) + 2HCl(aq) = ZnCl2(aq) + H2(g)��
2CrCl3(aq) + Zn(s)= 2CrCl2 (aq) + ZnCl2(aq)
2Cr2+(aq) + 4CH3COO��(aq) + 2H2O(l) = [Cr(CH3COO)2]2��2H2O (s)
��ش��������⣺
(1)����1�������� , ��ʢװ���Լ��� ��
(2)��ʵ�������õ���Һ�������õ�����ˮ����������У�ԭ���� ��
(3)ʵ�鿪ʼ����H2����, Ϊʹ���ɵ�CrCl2��Һ��CH3COONa��Һ˳����ϣ�Ӧ ����A�� ����B (�������������ر���)��
(4)��ʵ����п�����������ԭ���� �� ��
(5)��֪������Ӧ��������ʵ��ʱȡ�õ�CrCl3��Һ�к�����6.34 g��ʵ���ø��﴿����[Cr(CH3COO)2]2��2H2O 5.64 g��������ʵ�����ò�Ʒ�IJ��� ��
(6)��ʹ�ø�װ���Ʊ�Fe(OH)2�����ܽϳ�ʱ�俴��Fe(OH)2��ɫ������������1��2��3��Ӧװ����Լ�����Ϊ �� �� ��(д��ѧʽ)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com