
| ��Һ�б����������� | Fe3+ | Fe2+ | Cu2+ |
| ��ȫ������������� ��ʱ����Һ��pH | ��3.7 | ��6.4 | ��4.4 |


 �����ҵ���������ͯ������ϵ�д�
�����ҵ���������ͯ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������NaOH�Ѿ����� |
| B��������ƿ�м�ˮδ���̶��� |
| C��������NaOH��Һ�������ձ��� |
| D���ô������������ƽ��2.4gNaOHʱ�����ˡ������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ����ʽ | �ṹ��ʽ | ��� | �۵� | �ܽ��� |
| C12H10ClN3O |  | ��ɫ�ᾧ��ĩ | 170��172�� | ������ˮ |

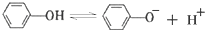 �����ӵ����Դ���
�����ӵ����Դ���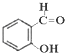 �����ǻ�����ȩ������ԭ����
�����ǻ�����ȩ������ԭ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��NH4Cl��Һ�У�c��Cl-��=c��NH4+����c��OH-��=c��H+�� |
| B��Na2SO4��Һ�У�c��Na+��+c��H+��=c��SO42-��+c��OH-�� |
| C��NaHCO3��Һ�У�c��Na+����c��HCO3-����c��CO32-����c��OH-�� |
| D��Ũ�Ⱦ�Ϊ0.1mol?L-1CH3COOH��CH3COONa��Һ�������ϣ�2c��H+��-2c��OH-��=c ��CH3COO-��-c��CH3COOH�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
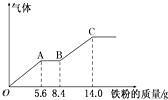 ijϡ�����ϡ����Ļ����Һ200mL��ƽ���ֳ����ݣ�������һ��������ͭ�ۣ�������ܽ�9.6g������һ�����������ۣ�������������������������ӵı仯��ͼ��ʾ����֪����ֻ����ԭΪNO���壩�����з�������������ǣ�������
ijϡ�����ϡ����Ļ����Һ200mL��ƽ���ֳ����ݣ�������һ��������ͭ�ۣ�������ܽ�9.6g������һ�����������ۣ�������������������������ӵı仯��ͼ��ʾ����֪����ֻ����ԭΪNO���壩�����з�������������ǣ�������| A��ԭ�������HNO3�����ʵ���Ϊ0.1 mol |
| B��OA�β�������NO��AB�εķ�ӦΪFe+2Fe3+�T3Fe2+��BC�β������� |
| C���ڶ�����Һ����������ΪFeSO4 |
| D��H2SO4Ũ��Ϊ2.5 mol?L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��25��ʱ������Mg��OH��2��Һ�뱥��MgF2��Һ��ȣ�ǰ�ߵ�c��Mg2+���� |
| B��25��ʱ��Mg��OH��2������Һ����������NH4Cl���壬c��Mg2+������ |
| C��25��ʱ��Mg��OH��2������20 mL 0.01 mol?L-1��ˮ�е�Ksp����20 mL 0.01 mol?L-1NH4Cl��Һ�е�KspС |
| D��25��ʱ����Mg��OH��2������Һ�м���NaF��Һ��Mg��OH��2������ת����ΪMgF2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Ҷ���أ���ɫ�� |
| B���������ƣ���ζ�� |
| C��̼���ƣ����ɼ� |
| D���������ƣ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��v��A��=0.5 mol?L-1?min-1 |
| B��v��B��=0.01 mol?L-1?s-1 |
| C��v��C��=0.8 mol?L-1?min-1 |
| D��v��D��=1 mol?L-1?min-1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com