
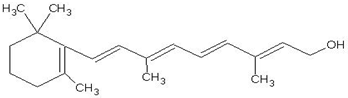
科目:高中化学 来源: 题型:解答题

 、C
、C .反应④所用试剂和条件是氢氧化钠醇溶液、加热.
.反应④所用试剂和条件是氢氧化钠醇溶液、加热. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HBrO3 | B. | XeF2 | C. | HBrO4 | D. | Xe |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
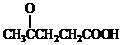 )合成聚芳酯E的路线:
)合成聚芳酯E的路线: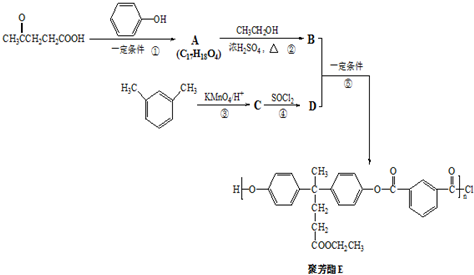
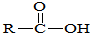 →
→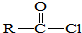 +SO2+HCl
+SO2+HCl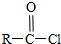 +R′OH→
+R′OH→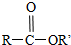 +HCl(R、R′表示烃基)
+HCl(R、R′表示烃基)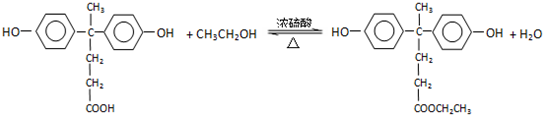 .
.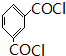 .
.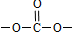 结构 ④苯环上只有2个取代基在上述同分异构体中,写出其中任一种与足量NaOH溶液共热反应的化学方式:
结构 ④苯环上只有2个取代基在上述同分异构体中,写出其中任一种与足量NaOH溶液共热反应的化学方式: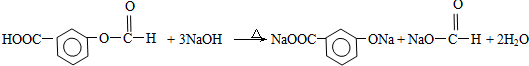 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | Cl2能与碱反应 | Cl2可用于制漂白粉 |
| B | Si有导电性 | SiO2可用于制光导纤维 |
| C | N2性质稳定 | N2可作为食品保护气 |
| D | 锌的金属性比铁强 | 轮船外壳上焊接若干锌块以减缓其腐蚀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
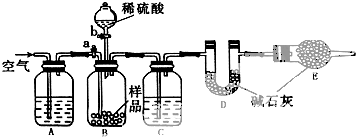
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+和Na+ | B. | Al3+和Cl- | C. | OH-和NH4+ | D. | H2S和CH4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com