
某学生想利用右图装置(烧瓶位置不能移动)收集下列气体:①H2; ②Cl2;③SO2;④HCl;⑤NH3;⑥NO;⑦NO2。下列说法正确的是 ( )

A.烧瓶是干燥的,由B进气,可收集②③④⑥⑦
B.烧瓶是干燥的,由A进气,可收集①⑤
C.在烧瓶中充满水,由A进气,可收集①⑤⑦
D.在烧瓶中充满水,由B进气,可收集⑥
科目:高中化学 来源:2017届福建省高三上学期开学考试化学试卷(解析版) 题型:填空题
已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子最外层电子数是内层电子数的3倍;E的+1价阳离子的核外有3层电子且各层均处于全满状态.
(1)E元素基态原子的核外电子排布式为 .
(2)B、C、D三种元素的第一电离能由小到大的顺序为 (填元素符号);
(3)B2A4是石油炼制的重要产物之一.B2A4分子中B原子轨道的杂化类型为 ;B2A4分子的空间构型是 ;1molB2A4分子中含σ键数目为 .
查看答案和解析>>
科目:高中化学 来源:2017届安徽省六安市高三上第一次月考化学试卷(解析版) 题型:选择题
某化学兴趣小组进行了有关Cu、硝酸、硫酸化学性质的实验,实验过程如下图所示。下列有关说法正确的是
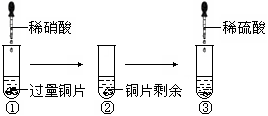
A.实验①中溶液呈蓝色,试管口有红棕色气体产生,说明稀硝酸被Cu还原为NO2
B.实验③中滴加稀硫酸,铜片继续溶解,说明稀硫酸的氧化性比稀硝酸强
C.实验③发生反应的化学方程式为:3Cu+Cu(NO3)2+4H2SO4=4CuSO4+2NO↑+4H2O
D.由上述实验可得出结论:Cu在常温下既可以和稀硝酸反应,也可以和稀硫酸反应
查看答案和解析>>
科目:高中化学 来源:2017届安徽省淮北市濉溪县高三上学期9月月考化学试卷(解析版) 题型:填空题
铁是世界上用量最大的金属,铁及其化合物在生活、生产中有广泛应用。
请回答下列问题:
⑴ Fe3O4是磁铁矿的主要成分,Fe3O4可用于制造录音磁带和电讯器材等。高温下,铝粉能与Fe3O4发生铝热反应,该反应的化学方程式为 。34.8g Fe3O4与足量稀硝酸反应,被还原HNO3的物质的量为 mol。
⑵ FeCl3溶液是一种黄色透明液体,可用作止血剂,其原因是
;向煮沸的蒸馏水中加入几滴饱和FeCl3溶液,继续煮沸得到红褐色的Fe(OH)3胶体,鉴别FeCl3溶液与Fe(OH)3胶体的方法是 。
⑶ 高铁酸钠(Na2FeO4)是一种绿色水处理剂,具有杀菌消毒和聚沉水中杂质的作用,它的杀菌消毒原理是 。高铁电池是一种新型可充电电池,高铁电池的总反应为3Zn+2Na2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4NaOH。该电池充电时阳极的电极反应式为 。
3Zn(OH)2+2Fe(OH)3+4NaOH。该电池充电时阳极的电极反应式为 。
⑷ 铁红是一种重要的红色颜料,其主要成分是Fe2O3,将一定量的铁红溶于130mL 5mol·L-1盐酸中,再加入一定量铁粉恰好溶解,收集到2.24L气体(标准状况),向反应后溶液中加入几滴KSCN溶液,溶液不变红色,则参加反应的铁粉质量为 。
查看答案和解析>>
科目:高中化学 来源:2017届安徽省淮北市濉溪县高三上学期9月月考化学试卷(解析版) 题型:选择题
把等物质的量的CuSO4、FeCl3和锌粉置于足量的水中,充分反应,反应后的溶液中大量存在的金属阳离子是( )
A.Cu2+、Fe3+、Fe2+、Zn2+ B.Fe3+、Fe2+、Zn2+
C.Cu2+、Fe3+、Zn2 + D.Cu2+、Fe2+、Zn2+
查看答案和解析>>
科目:高中化学 来源:2017届河南省濮阳市高三上第二次检测化学试卷(解析版) 题型:推断题
如图所示是某些无机物的转化关系(部分反应物和生成物未列出)。已知F是一种红褐色沉淀;M、K是常见的金属单质;B是一种有刺激性气味的气体;向C溶液中加入BaCl2溶液,生成不溶于稀盐酸的白色沉淀。

(1)已知盐X不带结晶水,则X的化学式为_________。
(2)若不考虑损失,G、D和H2O可恰好完全反应生成I,反应时G和D的物质的量之比为__________。
(3)足量K与I的稀溶液反应的离子方程式为____________________。
(4)J与NaOH溶液恰好完全反应可生成一种盐。将该盐的水溶液蒸干灼烧可得到_________(填化学式)。
(5)在0.02 mol·L-1的X溶液中,各种离子的浓度由大到小的顺序为_______________。
查看答案和解析>>
科目:高中化学 来源:2017届河南省灵宝市高三上学期9月月考化学试卷(解析版) 题型:选择题
研究发现,硝酸越稀,还原产物中氮元素的化合价越低。某同学取适量的铁铝合金与足量很稀的硝酸充分反应,没有气体放出。在反应结束后的溶液中,逐滴加入4 mol/LNaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。下列说法不正确的是
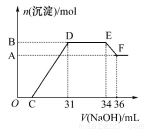
A.OC段离子反应方程式:H++OH-=H2O
B.溶液中结合OH-能力最强的离子是H+,最弱的离子是Al3+
C.溶液中n(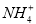 )=0.012 mol
)=0.012 mol
D.欲测定F点沉淀的质量,实验步骤是过滤、洗涤、干燥、称量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com