
����Ŀ������ѧ��ѡ��3�����ʽṹ�����ʡ�
2015���ҹ��������Ƶ�C919���Ϳͻ���ʽ��������־���ҹ���Ϊ�������������������з�������Ϳͻ������Ĺ��ң�ͬʱ��ζ���й��߶�װ������ҵ��չ��һ��ȫ�µĸ߶ȡ�
��1���ɻ������ͨ������þ�������ѺϽ���ϣ��ѵļ۵����Ų�ͼΪ__________����һ�����ܣ�þ _________������������������С��������
��2��Fe��CO���γ�������ʻ���[Fe��CO��5]���÷���������������������Ϊ________��
��3��SCl2�����е�����ԭ���ӻ����������_______���÷��ӹ���Ϊ_________��
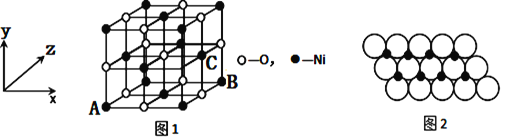
��4����֪MgO��NiO�ľ���ṹ����ͼ1����ͬ������Mg2+��Ni2+�����Ӱ뾶�ֱ�Ϊ66pm��69 pm�����۵㣺MgO_____NiO������>������<������=������������_____________��
��5����ͼ����ʾ��NiO�����������������AΪ��0��0��0����BΪ��1��0��1������C�����������Ϊ___________��
��6��һ���¶��£�NiO��������Է��ط�ɢ���γ��������Ӳ�����������ΪO2�������õ������У�Ni2+������У���ͼ2������֪O2���İ뾶Ϊa m��ÿƽ��������Ϸ�ɢ�ĸþ��������Ϊ______g������a��NA��ʾ��
���𰸡� ![]() ���� 1��1 sp3 V�λ������ξ��� > �������������ͬ��Mg2+�뾶��Ni2+С������MgO�ľ����ܱ�NiO����MgO�۵�� ��1��
���� 1��1 sp3 V�λ������ξ��� > �������������ͬ��Mg2+�뾶��Ni2+С������MgO�ľ����ܱ�NiO����MgO�۵�� ��1�� ![]() ��
�� ![]() ����1,0.5,0.5��
����1,0.5,0.5�� ![]() ��
��![]() ��
��![]()
��������(1).��Ϊ22��Ԫ�أ��۵����Ų�Ϊ3d24s2���۵����Ų�ͼΪ![]() ��þԪ�ص�3s�ܼ�Ϊȫ���ȶ�״̬�������ϵͣ�þ�ĵ�һ�����ܴ������ģ��ʴ�Ϊ��
��þԪ�ص�3s�ܼ�Ϊȫ���ȶ�״̬�������ϵͣ�þ�ĵ�һ�����ܴ������ģ��ʴ�Ϊ�� ![]() �����ڣ� (2) Fe��CO���γ�������ʻ���[Fe��CO��5]��ÿ��CO�к���1��������2���м������Ը÷�����������4+4=8���м���4�������Զ��߱���Ϊ1:1���ʴ�Ϊ�� 1��1�� (3). SCl2��������ԭ���ӻ������Ϊ��6+2��/2=4����ȡsp3�ӻ���ʽ�����ӹ¶Ե��Ӷԣ����Ը÷��ӹ���ΪV�λ������Σ��ʴ�Ϊ��sp3 ��V�λ������ξ��ɣ� (4). ����Mg2+��Ni2+�����Ӱ뾶�ֱ�Ϊ66pm��69 pm���������ӵ����ͬʱ�����Ӱ뾶ԽС��������Խ�������MgO�۵����NiO���۵㣬�ʴ�Ϊ�� >���������������ͬ��Mg2+�뾶��Ni2+С������MgO�ľ����ܱ�NiO��MgO�۵�ߣ� (5) NiO�����������������AΪ��0��0��0����BΪ��1��0��1������C���ӵ�xϵ�����Bx������ͬ��yzϵ���궼���е��ϣ�����C�����������Ϊ��1��
�����ڣ� (2) Fe��CO���γ�������ʻ���[Fe��CO��5]��ÿ��CO�к���1��������2���м������Ը÷�����������4+4=8���м���4�������Զ��߱���Ϊ1:1���ʴ�Ϊ�� 1��1�� (3). SCl2��������ԭ���ӻ������Ϊ��6+2��/2=4����ȡsp3�ӻ���ʽ�����ӹ¶Ե��Ӷԣ����Ը÷��ӹ���ΪV�λ������Σ��ʴ�Ϊ��sp3 ��V�λ������ξ��ɣ� (4). ����Mg2+��Ni2+�����Ӱ뾶�ֱ�Ϊ66pm��69 pm���������ӵ����ͬʱ�����Ӱ뾶ԽС��������Խ�������MgO�۵����NiO���۵㣬�ʴ�Ϊ�� >���������������ͬ��Mg2+�뾶��Ni2+С������MgO�ľ����ܱ�NiO��MgO�۵�ߣ� (5) NiO�����������������AΪ��0��0��0����BΪ��1��0��1������C���ӵ�xϵ�����Bx������ͬ��yzϵ���궼���е��ϣ�����C�����������Ϊ��1�� ![]() ��
�� ![]() ����1,0.5,0.5�����ʴ�Ϊ��1��
����1,0.5,0.5�����ʴ�Ϊ��1�� ![]() ��
�� ![]() ����1,0.5,0.5�� (6)����ͼƬ��֪��ÿ����������ռ�����Ϊ
����1,0.5,0.5�� (6)����ͼƬ��֪��ÿ����������ռ�����Ϊ![]() ����ÿƽ�����е�����������=
����ÿƽ�����е�����������=![]() ��ÿ��������������=
��ÿ��������������=![]() ������ÿƽ�����е�����������=
������ÿƽ�����е�����������=![]() ��
��![]() =
=![]() ���ʴ�Ϊ��
���ʴ�Ϊ�� ![]() ��
��![]() ��
��![]() ��
��


 ֥�鿪���γ�������ϵ�д�
֥�鿪���γ�������ϵ�д� ����ѧ��ţ��Ӣ��ϵ�д�
����ѧ��ţ��Ӣ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��20��ʱ������KCl��Һ���ܶ�Ϊ1.174gcm��3 �� ���ʵ���Ũ��Ϊ4.0molL��1 �� ������˵���в���ȷ���ǣ� ��
A.25��ʱ������KCl��Һ��Ũ�ȴ���4.0 mol?L��1
B.����Һ��KCl����������Ϊ ![]()
C.20��ʱ���ܶ�С��1.174g?cm��3��KCl��Һ�Dz�������Һ
D.������Һ��������ˮ���ٻָ���20��ʱ����Һ�ܶ�һ������1.174g?cm��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��ȷ���ǣ� ��
A.Cl2ͨ��ˮ�У�Cl2+H2O�T2H++Cl��+ClO��
B.˫��ˮ�м���ϡ�����KI��Һ��H2O2+2H++2I���TI2+2H2O
C.��ͭ���缫���CuSO4��Һ��2Cu2++2H2O ![]() 2Cu+O2��+4H+
2Cu+O2��+4H+
D.Na2S2O3��Һ�м���ϡ���2S2O ![]() +4H+�TSO
+4H+�TSO ![]() +3S��+2H2O
+3S��+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʽ�����ˮ���ɼ������(����)
A.�Ҵ����ױ����屽
B.�Ҵ��������ױ�
C.���顢��ϩ����Ȳ
D.����ϩ�����Ȼ�̼��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����е��뷽��ʽ��ȷ���ǣ� ��
A.CuCl2�TCu2++Cl2��
B.Al2��SO4��3=2Al3++3SO ![]()
C.Fe2��SO4��3�T2Fe2++3SO ![]()
D.Ba��NO3��2�TBa2++2��NO3��2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2L���ܱ������У��������»�ѧ��Ӧ��CO2(g)��H2(g) ![]() CO(g)��H2O(g)���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
CO(g)��H2O(g)���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
t�� | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�ش��������⣺
��1���÷�ӦΪ_______��Ӧ��ѡ�����ȡ����ȣ���
��2�����жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬��������_______��
A��������ѹǿ���� B.��������� c(CO)����
C.v��(H2)��v��(H2O) D.c(CO2)��c(CO)
��3��ij�¶��£�ƽ��Ũ�ȷ�����ʽ��c(CO2)��c(H2)��c(CO)��c(H2O)�����жϴ�ʱ���¶�Ϊ____�档���¶��£�����������г���n(CO2)=1mol, n(H2)=1mol,4minĩ�ﵽƽ�⣬CO2��ת����Ϊ_______��H2���������Ϊ________________��
��4��д�������淴Ӧ���ʵĴ�ʩ��___________________��������д���֣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijԭ����ܷ�Ӧ�����ӷ���ʽΪ2Fe3++Fe=3Fe2+ �� ����ʵ�ָ÷�Ӧ��ԭ�������ǣ� ��
A.����Ϊͭ������Ϊ�����������ҺΪFeCl3��Һ
B.����Ϊ̼������Ϊ�����������ҺΪFe��NO3��3��Һ
C.����Ϊ��������Ϊ�����������ҺΪFe2��SO4��3��Һ
D.����Ϊ��������Ϊ�����������ҺΪCuSO4��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1.85g��п������ͭ�ĺϽ���������������У���Ӧ��Ϻ�448mL����������������ڴ˺Ͻ����ɣ�����˵���в���ȷ���ǣ� ��
A.�Ͻ�������п�����ʵ���֮��Ϊ0.02mol
B.�Ͻ���ͭ��������ȷ��
C.�Ͻ�������ͭ�����ʵ���֮��Ϊ0.01mol
D.1.30g������п����֮�ͣ�1.12g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����г�ȥ���ʣ������ڵ�����Ϊ���ʣ��ķ����д������
A. FeSO4��CuSO4�������������ۺ���
B. CO ��CO2������NaOH��Һϴ�������
C. CO2��HCl������NaOH��Һϴ�������
D. MnO2��KCl������ˮ�ܽ���ˡ�ϴ�ӡ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com