
| A. | 有大量的氯气泄漏时,用肥皂水浸湿软布蒙面,并迅速离开现场 | |
| B. | 金属钠着火燃烧时,用泡沫灭火器灭火 | |
| C. | NaCl必须保存在棕色瓶中 | |
| D. | 含硫酸的废液倒入水槽,用水冲入下水道 |
分析 A.氯气有毒,属于酸性气体,能和碱性物质反应;
B.钠和水、氧气反应,钠燃烧生成过氧化钠,过氧化钠和二氧化碳、水反应生成氧气;
C、氯化钠性质很稳定;
D、硫酸具有腐蚀性,用水冲入下水道会污染地下水.
解答 解:A.氯气有毒,属于酸性气体,能和弱碱性的肥皂水反应,故A正确;
B.钠和水反应生成氢气,氢气是易燃物,钠燃料后生成过氧化钠,过氧化钠和水、二氧化碳反应生成氧气,促进钠的燃烧,所以钠着火燃烧时,不能用泡沫灭火器灭火,应该用沙子灭火,故B错误;
C、氯化钠性质很稳定,见光不分解,故不必保存在棕色的试剂瓶中,故C错误;
D、含硫酸的废液没有经过处理后不能直接倒入水槽,应先导入废液缸中集中回收处理,故D错误.
故选A.
点评 本题考查了化学实验中的安全及事故处理知识,题目难度不大,旨在考查学生的基础知识的掌握,化学实验是化学的基础,要了解常见的实验操作,能对错误操作的后果做出判断,养成良好的实验习惯.


科目:高中化学 来源: 题型:选择题
| A. | 若反应物键能之和大于生成物键能之和,则该反应为放热反应 | |
| B. | 含有共价键的化合物一定是共价化合物 | |
| C. | 因为水分子内存在氢键,所以水的沸点比硫化氢的沸点高 | |
| D. | 需要加热才能发生的化学反应不一定是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,1mol水的体积是22.4L | |
| B. | 在标准状况下,22.4L氦气所含的原子数约为2NA | |
| C. | 同温同压下,等体积的硫酸和硝酸所含氢原子数之比为2:1 | |
| D. | 1molCxHy分子中所含C-H数目为yNA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

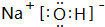
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 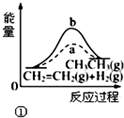 图①中a、b曲线分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g)+△Q,0<△Q;使用和未使用催化剂时,反应过程中的能量变化 | |
| B. | 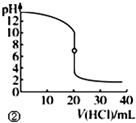 图②表示25℃时,用0.01mol•L-1盐酸滴定一定体积的0.01mol•L-1 NaOH溶液,溶液的pH随加入酸体积的变化 | |
| C. | 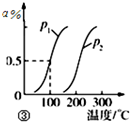 图③表示CH4(g)+H2O(g)?CO(g)+3H2(g)+△Q,反应CH4的转化率与温度、压强的关系,且p1>p2、0<△Q | |
| D. | 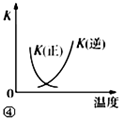 图④中曲线表示反应2SO2(g)+O2(g)?2SO3(g)+△Q,0<△Q;正、逆反应的平衡常数K随温度的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D |
 | 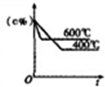 | 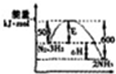 | 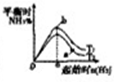 |
| P代表的是压强 | c%是氨气百分含量 | 1molN2和3molH2反应达平衡放出热量92kJ | 平衡常数:Kb>Ka |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
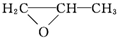 +H2O→
+H2O→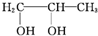 .
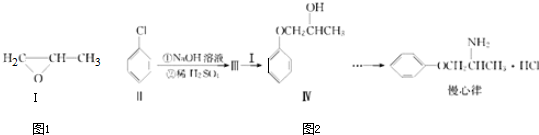
.
 .
.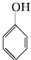 +3Br2→
+3Br2→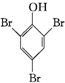 ↓+3HBr.
↓+3HBr.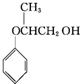 .
.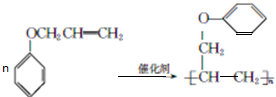 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制氯气盛放在棕色试剂瓶中,存放于低温避光的地方 | |
| B. | 固体碘常盛放在棕色细口瓶中 | |
| C. | 液溴易挥发,盛放在用水液封的棕色试剂瓶中 | |
| D. | 金属钠易被氧化,少量金属钠应储存在煤油中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(B)=0.03mol•L-1•s-1 | B. | v(B)=0.045mol•L-1•s-1 | ||
| C. | v(C)=0.03mol•L-1•s-1 | D. | v(C)=0.06mol•L-1•s-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com