
为测定某镁铝合金的成分,取14.7g合金完全溶于500mL3mol·L-1的硫酸中,现加入400mL 8mol·L-1的NaOH溶液充分反应,得到白色沉淀。
1)、 若只有一种沉淀,试确定合金中镁的质量分数范围。
2)、若沉淀质量为26.3g,则镁的质量分数为多少?
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
| ||
| ||
| 9b |
| 17a |
| 9b |
| 17a |
查看答案和解析>>
科目:高中化学 来源:2012-2013年福建霞浦一中高一下学期第一次月考化学试卷(带解析) 题型:实验题
某铝合金中含有单质铝、镁、铜、硅,为了测定该合金中铝的含量,设计了如下实验流程,请回答有关问题: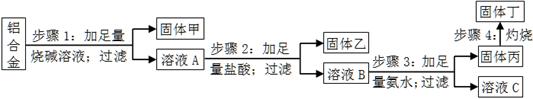
(1)步骤1所得固体甲的成分为 。
(2)步骤2中加足量盐酸,而不采用通入足量二氧化碳的原因为 。
(3)步骤3中生成固体丙的离子方程式为 ;溶液C中所含有的阳离子符号为 。
(4)步骤4所发生反应的化学方程式为 。
(5)现用托盘天平称取10.0g铝合金进行上述流程图所示操作,所得固体丁质量为15.3g,则该铝合金中铝的质量分数为 ;并判断以下操作对铝质量分数测定的影响(填“偏大”、“偏小”或“无影响”)。
a.步骤1中烧碱量不足,则 ;
b.步骤4中灼烧不充分,则 。
查看答案和解析>>
科目:高中化学 来源:2015届福建霞浦一中高一下学期第一次月考化学试卷(解析版) 题型:实验题
某铝合金中含有单质铝、镁、铜、硅,为了测定该合金中铝的含量,设计了如下实验流程,请回答有关问题:
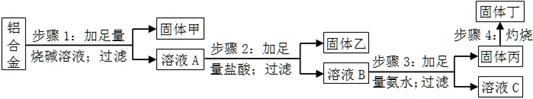
(1)步骤1所得固体甲的成分为 。
(2)步骤2中加足量盐酸,而不采用通入足量二氧化碳的原因为 。
(3)步骤3中生成固体丙的离子方程式为 ;溶液C中所含有的阳离子符号为 。
(4)步骤4所发生反应的化学方程式为 。
(5)现用托盘天平称取10.0g铝合金进行上述流程图所示操作,所得固体丁质量为15.3g,则该铝合金中铝的质量分数为 ;并判断以下操作对铝质量分数测定的影响(填“偏大”、“偏小”或“无影响”)。
a.步骤1中烧碱量不足,则 ;
b.步骤4中灼烧不充分,则 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某铝合金(硬铝)中含有镁、铜、硅,为了测定该合金中铝的含量,有人设计如下实验过程(实验前已经将合金样品磨成粉末状)
(1)称取样品a g,称取时使用的仪器名称为 。
(2)将上述样品溶解于足量稀盐酸中,过滤,滤渣中含有
(3)在滤液中加过量NaOH溶液,过滤。
(4)在第(3)步的滤液中通入足量的CO2,充分反应后过滤,将沉淀用蒸馏水洗涤数次后烘干灼烧至质量不再减少为止。冷却后称量,质量为b g。有关反应的离子方程式为 ,该样品中铝的质量分数为
(5)①若步骤(3)中NaOH溶液的量加入不足,则能使测定结果 (填“偏高”、“偏低”或“不影响”)。
②若步骤(4)中沉淀没有洗涤,则能使测定结果 (填“偏高”、“偏低”或“不影响”)。
查看答案和解析>>
科目:高中化学 来源:2008-2009学年山东省临沂市费县高三(上)期中化学试卷(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com