
【题目】某有机物的结构简式如图所示, 下列说法中不正确的是( )
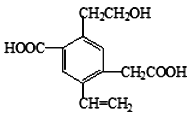
A. 1mol该有机物和过量的金属钠反应最多可以生成1.5 molH2
B. 该有机物消耗Na、NaOH、NaHCO3的物质的量之比为3∶2∶2
C. 可以用酸性KMnO4溶液检验其中的碳碳双键
D. 该有机物能够在催化剂作用下发生酯化反应
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】短周期主族元素X﹑Y﹑Z﹑W﹑Q的原子序数逐渐增大。X原子核外最外层电子数是次外层电子数的2倍。Y的氟化物YF3分子中各原子均满足最外层8电子稳定结构。Z﹑W是常见金属,Z是同周期中原子半径最大的元素。W的简单离子是同周期中离子半径最小的。X和Z原子序数之和与Q的原子序数相等。下列说法正确的是
A. 相同质量的Z和W单质分别与足量稀盐酸反应时,Z的单质获得的氢气多
B. X与Q形成的化合物和Z与Q形成的化合物的化学键类型相同
C. 最高价氧化物对应的水化物的酸性:X<W
D. Y的简单气态氢化物与Q的单质反应,现象是产生白烟
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应,其中①②③属于同种反应类型。根据如图回答下列问题:
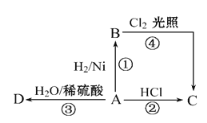
(1)写出A、B、C、D的结构简式:A__,B__,C__,D__。
(2)写出②、④两步反应的化学方程式,并注明反应类型。
②_________________,反应类型________。
④_________________,反应类型________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应2HI(g)![]() H2(g) +I2(g)的能量变化如图所示。下列说法正确的是
H2(g) +I2(g)的能量变化如图所示。下列说法正确的是

A. 常温下,向体积为VL的容器中充入2mol HI(g)充分反应,可吸收12.5kJ的热量
B. 加入催化剂,分子的能量不变,但单位体积活化分子数增多,速率加快
C. 其他条件不变,升高温度,反应速率加快,HI分解率不变
D. H2(g) +I2(g)![]() 2HI(g)的活化能Ea为12.5kJ·mol1
2HI(g)的活化能Ea为12.5kJ·mol1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图为元素周期表中短周期的一部分,关于Y、Z、M的说法正确的是
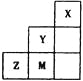
A. 非金属性:![]()
B. 离子半径:![]()
C. ZM2分子中各原子的最外层均满足8电子稳定结构
D. 三种元素中,Y的最高价氧化物对应的水化物酸性最强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答问题:
(1)除去下列表格物质中的杂质(括号中是杂质),从所给试剂及操作方法中选出合适的药品及方法(填序号):
除杂试剂:A.溴水 B.饱和碳酸钠溶液 C.氢氧化钠溶液 D.乙醇
操作方法:E.蒸馏 F.分液 G.洗气 H.萃取
物质(括号中是杂质) | 除杂试剂 | 操作方法 |
①硝基苯(硝酸) | _____ | _____ |
②乙酸乙酯(乙酸) | _____ | _____ |
③甲烷(乙烯) | _____ | _____ |
(2)①乙酸中官能团的名称是__________________。
②工业上用乙烯水化法制备乙醇,反应的化学方程式是______________。
③红热的铜丝插入乙醇中反复几次发生反应,反应的化学方程式是______________,该反应类型为___________反应。
④丁烷有___________种同分异构体,其中___________(写名称)熔、沸点较低。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下列实验装置进行相应的实验(部分夹持装置略去),不能达到实验目的的是
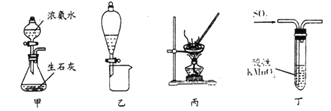
A. 利用图甲装置可快速制取少量氨气
B. 利用图乙装置分离水和溴的苯溶液
C. 利用图丙装置蒸发KCl溶液得晶体
D. 图丁装置中溶液颜色变浅,说明SO2具有漂白性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴的化合物在磁性材料生产、电池制造、催化剂制备等方面应用十分广泛。
(1)二价钴离子的核外电子排布式为______。基态Co原子核外3d能级上有______个未成对电子。Co与Ca属同周期,且核外最外层电子构型相同,但金属钴熔沸点都比钙高,原因是______。
(2)0.1mol[Co(NO2)6]3-中所含的σ键数目是______,K3[Co(NO2)6]中K、N、O三种元素的第一电离能由大到小的顺序是______。
(3)化合物四氨基钴酞菁分子的结构式如图。四氨基钴酞菁中N原子的杂化轨道类型为______。
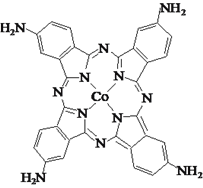
(4)[Co(NH3)6]Cl3晶体可由CoCl2溶于氨水并通入空气制得,该配合物中配体分子的立体构型是______。
(5)一种钴的化合物可用作石油脱硫的催化剂,其晶胞结构如图所示,则晶体中与每个O2-紧邻的O2-有______个,该钴的化合物的化学式是______。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com