
下列对阿伏加德罗常数的叙述中,正确的是( )
①阿伏加德罗常数就是6.02×1023 mol-1
②阿伏加德罗常数为1 mol指定粒子的粒子数
③阿伏加德罗常数为12 g碳所含的碳原子数
④阿伏加德罗常数用符号NA表示,其值约为6.02×1023 mol-1
A.①② B.①③ C.②③ D.②④
 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源: 题型:
某气体分子,其摩尔质量为M g/mol,该气体的体积为V L(标况)溶于1L水中,形成溶液的密度为d g /cm3 设阿伏加德罗常数的值为NA 则:
①该气体的物质的量为________ mol;(用含d 、 V 、M的代数式表示,下同) ②该溶液中溶质的质量分数________; ③该气体在标准状况下的密度为________g/L; ④该溶液中溶质的物质的量浓度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
SO2溶于水后所得溶液的性质是( )
A.有氧化性,无还原性,无酸性 B.有氧化性,有还原性,有酸性
C.有还原性,无氧化性,无酸性 D.有还原性,无氧化性,有酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
A~H等8种物质存在如下图所示转化关系(反应条件、部分产物未标出)。已知:A是正盐,B是能使品红溶液退色的气体,G是红棕色气体。按要求回答问题:

(1)写出下列物质的化学式:
A________,B________,E________。
(2)写出下列反应的化学方程式:
G―→H+F_____________________________________________;
D的浓溶液与木炭反应的化学方程式:____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某溶液中Cl-、Br-、I-的物质的量之比为2∶3∶4,现欲使溶液中Cl-、Br-、I-的物质的量之比为4∶3∶2,那么要通入Cl2的物质的量是原溶液中I-的物质的量的( )
A.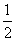 B.
B.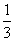
C.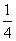 D.
D.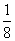
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关阿伏加德罗常数的说法正确的是( )
A.阿伏加德罗常数是国际单位制中七个基本物理量之一
B.1 mol任何物质都约含有6.02×1023个原子
C.阿伏加德罗常数约为6.02×1023 mol-1
D.阿伏加德罗常数没有单位
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于物质的量的叙述中,正确的是( )
A.1 mol 任何物质都含有6.02×1023个分子
B.0.012 kg 14C中约含有6.02×1023个碳原子
C.1 mol水中含有2 mol氢和1 mol氧
D.1 mol Ne 约含有6.02×1024个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25℃时有关物质的电离平衡常数:
| 弱酸 | CH3COOH | 苯酚 | H2CO3 |
| 电离平衡常数 | 1.75×l0–5 | 1.1×l0–10 | K1=4.4×l0–7 K2=4.7×l0–11 |
下列叙述错误的是
A.等物质的量浓度的各溶液pH关系为:
pH(C6H5ONa)>pH(Na2CO3)>pH(NaHCO3)>pH(CH3COONa)
B.向苯酚钠溶液中通入少量CO2气体反应为:C6H5O– +H2O + CO2 →C6H5OH +HCO3-
C.等物质的量浓度的苯酚稀溶液与 NaOH稀溶液等体积混合后溶液中:
c(Na+)>c(C6H5O–)>c(OH–)>c(H+)
D.NaHCO3和Na2CO3混合液中,一定有c(Na+)+ c(H+)=c(OH–)+ c(HCO3–) +2c(CO32–)
查看答案和解析>>
科目:高中化学 来源: 题型:
制烧碱所用盐水需两次精制。第一次精制主要是用沉淀法除去粗盐水中Ca2+、Mg2+、Fe3+、SO42-等离子,过程如下:
Ⅰ.向粗盐水中加入过量BaCl2溶液,过滤;
Ⅱ.向所得滤液中加入过量Na2CO3溶液,过滤;
Ⅲ.滤液用盐酸调节pH,获得一次精制盐水。
(1)过程Ⅰ、Ⅱ生成的部分沉淀及其溶解度(20℃/g)如下表:
| CaSO4 | Mg2(OH)2CO3 | CaCO3 | BaSO4 | BaCO3 |
| 2.6×10-2 | 2.5×10-4 | 7.8×10-4 | 2.4×10-4 | 1.7×10-3 |
①检测Fe3+是否除尽的方法是________________________________________。
②过程Ⅰ选用BaCl2而不选用CaCl2,运用表中数据解释原因____________________。
③检测Ca2+、Mg2+、Ba2+是否除尽时,只需检测_______(填离子符号)。
(2)第二次精制要除去微量的I-、IO3-、NH4+、Ca2+、Mg2+,流程示意如下:
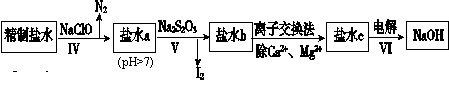

①过程Ⅳ除去的离子是________________。
②过程VI中,在电解槽的阴极区生成NaOH,结合化学平衡原理解释:___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com