
标准状况的温度和压强是()
A. 20℃,101kPa B. 0℃,101Pa C. 25℃,101kPa D. 0℃,101kPa
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
下列给出14种元素的电负性:
元素 Al B Be C Cl F Li Mg N Na O P S Si
电负性 1.5 2.0 1.5 2.5 3.0 4.0 1.0 1.2 3. 0 0.9 3.5 2.1 2.5 1.8
请运用元素周期律知识完成下列各题.
(1)同一周期中,从左到右,元素的电负性逐渐 ;同一主族中,从上到下,元素的电负性逐渐 .所以,元素的电负性随原子序数的递增呈 变化.
(2)短周期元素中,由电负性最大的元素与电负性最小的元素形成的化合物的化学式为NaF,用电子式表示该化合物的形成过程: .
(3)表中符合“对角线规则”的元素有Li和 、Be和 、B和 ,它们的性质分别有一定的相似性,其原因是 ,写出Be(OH)2与强酸及强碱反应的离子方程式: .
(4)一般认为,两成键元素间电负性差值大于1.7时形成离子键,两成键元素间电负性差值小于1.7时,形成共价键.判断Mg3N2、SO2、AlCl3、CS2、MgO是离子化合物还是共价化合物.
离子化合物 、共价化合物 .
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列化学方程式中,不能用离子方程式Ba2++SO42﹣=BaSO4↓表示的是()
A. BaCl2+H2SO4=BaSO4↓+2HCl
B. Ba(OH)2+Na2SO4=BaSO4↓+2NaOH
C. Ba(NO3)2+H2SO4=BaSO4↓+2HNO3
D. Ba(OH)2+H2SO4=BaSO4↓+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
某食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4 等杂质,通过如下几个实验步骤,可制得纯净的食盐水:
①加入稍过量的Na2CO3溶液;
②加入稍过量的NaOH溶液;
③加入稍过量的BaCl2溶液;
④滴入稀盐酸至无气泡产生;
⑤过滤;
正确的操作顺序是()
A. ③②①⑤④ B. ①②③⑤④ C. ②③①⑤④ D. ③⑤②①④
查看答案和解析>>
科目:高中化学 来源: 题型:
水溶液中能大量共存的一组离子是( )
A. NH4+、Ba2+、Br﹣、CO32﹣ B. Cl﹣、SO32﹣、Fe2+、H+
C. K+、Na+、SO42﹣、MnO4﹣ D. Na+、H+、NO3﹣、HCO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示的A、B两个电解池中的电极均为铂,在A池中加入0.05mol•L﹣1的CuCl2溶液,B池中加入0.1mol•L﹣1的AgNO3溶液,进行电解.a、b、c、d四个电极上所析出的物质的物质的量之比是()
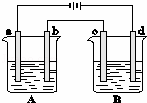
A. 1:1:2:1 B. 2:1:1:1 C. 2:2:4:1 D. 2:1:2:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com