
| A. | 自来水中通入Cl2用于杀菌、消毒是利用HClO的性质 | |
| B. | 用氯气消毒过的水可用于配制澄清石灰水溶液 | |
| C. | 氯水、液氯、氯气的成分相同,Cl2和Cl-的化学性质也相同 | |
| D. | 久制的氯水呈无色,但仍然有漂白、杀菌的功能 |
分析 A.HClO具有强氧化性,能杀菌消毒;
B.氯气消毒过的水含有HCl、氯气等;
C.液氯、氯气的成分为Cl2,氯水的成分为HCl、HClO、Cl2等;
D.久制的氯水,HClO分解生成盐酸.
解答 解:A.HClO具有强氧化性,能杀菌消毒,所以自来水中通入Cl2与水反应生成HClO,则杀菌、消毒是利用HClO的性质,故A正确;
B.氯气消毒过的水含有HCl、氯气等,用氯气消毒过的水,可与澄清石灰水发生反应,故B错误;
C.液氯、氯气的成分为Cl2,氯水的成分为HCl、HClO、Cl2等,Cl2具有氧化性,Cl-具有还原性,所以Cl2和Cl-的化学性质不相同,故C错误;
D.久制的氯水,HClO分解生成盐酸,盐酸没有漂白、杀菌的功能,故D错误.
故选A.
点评 本题考查了氯水的成分和性质、氯气的性质,题目难度不大,注意根据氯水中含有的粒子分析其性质.


科目:高中化学 来源: 题型:选择题
| A. | 金属钠着火时使用泡沫灭火器灭火 | |
| B. | 用试管加热碳酸氢钠固体时使试管口竖直向上 | |
| C. | 浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗 | |
| D. | 做蒸馏实验时,如果在沸腾前发现忘记加沸石,应立即停止加热,冷却后补加 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
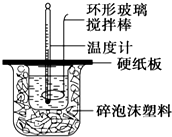 某实验小组设计用50mL 1.0mol/L盐酸跟50mL 1.1mol/L 氢氧化钠溶液在如图装置中进行中和反应.在大烧杯底部垫碎泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:
某实验小组设计用50mL 1.0mol/L盐酸跟50mL 1.1mol/L 氢氧化钠溶液在如图装置中进行中和反应.在大烧杯底部垫碎泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:| 实验序号 | 起始温度t1/℃ | 终止温度(t2)/℃ | 温差 (t2-t1)/℃ | ||
| 盐酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 31.6 | 6.6 |
| 2 | 25.1 | 25.1 | 25.1 | 31.8 | 6.7 |
| 3 | 25.1 | 25.1 | 25.1 | 31.9 | 6.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②④⑤ | C. | ①④⑤ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

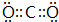 ;N的最高价氧化物与NaOH溶液反应离子方程式:SiO2+2OH-=SiO32-+H2O.
;N的最高价氧化物与NaOH溶液反应离子方程式:SiO2+2OH-=SiO32-+H2O.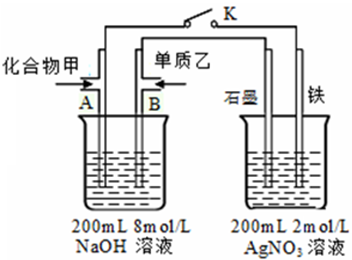
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 熔点:Br2>Cl2>F2 | B. | 氧化性:Cl2>Br2>I2 | ||
| C. | 酸性:HClO4>HBrO4>HIO4 | D. | 稳定性:HI>HBr>HCl>HF |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过渡元素全部是副族元素 | |
| B. | 周期表中的周期分为:短周期、长周期 | |
| C. | 周期表中的族分为:主族、副族、0族和VIII族 | |
| D. | 由短周期元素和长周期元素共同组成的族称为主族(除0族外) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
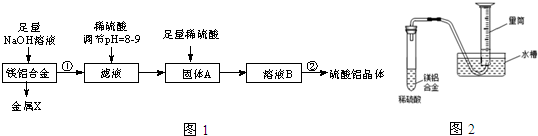
 ,固体A的化学式为Al(OH)3;
,固体A的化学式为Al(OH)3;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com