
| A、1mol FeI2与足量氯气反应时转移的电子数为2NA |
| B、2L 0.5mol?L-1硫酸钾溶液中阴离子所带电荷数为NA |
| C、1mol Na2O2固体中含离子总数为4NA |
| D、丙烯和环丙烷组成的42g混合气体中氢原子的个数为6NA |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
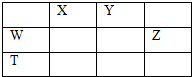
| A、X、Y、Z三种元素最低价氢化物的沸点依次升高 |
| B、由X、Y和氢三种元素形成的化合物中只有共价键 |
| C、物质WY2,W3X4,WZ4均有熔点高,硬度大的特性 |
| D、T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、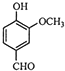 |
B、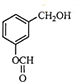 |
C、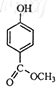 |
D、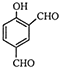 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该溶液中所含的离子是:Fe2+、K+、SO42-、NO3- |
| B、实验③,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为18g |
| C、若向该溶液中加入过量的稀硫酸,产生的气体遇空气能变成红棕色 |
| D、若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液会显血红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:O>N>C |
| B、酸性:HClO4>H2SO4>H3PO4 |
| C、稳定性:HCl>HI>HBr |
| D、金属性:Al>Mg>Na |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铁表面镀锌可增强其抗腐蚀性 |
| B、用聚乙烯塑料代替聚乳酸塑料可减少白色污染 |
| C、大量燃烧化石燃料是造成雾霾天气的一种重要因素 |
| D、含重金属离子的电镀废液不能随意排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、Ca2+、Cl-、SO42- |
| B、Fe2+、H+、SO32-、ClO- |
| C、Mg2+、NH4+、Cl-、SO42- |
| D、K+、Fe3+、NO3-、SCN- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分子式为C4H8含碳碳双键的同分异构体(包括顺反异构)共有5种 |
| B、甲苯能使酸性高锰酸钾溶液褪色,而甲基环己烷不能,说明有机物分子中的基团间存在相互影响 |
C、芥子醇(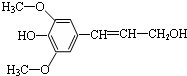 )能发生氧化、取代、水解、加聚反应 )能发生氧化、取代、水解、加聚反应 |
| D、将少量某物质的溶液滴加到新制的银氨溶液中,水浴加热后有银镜生成,该物质一定属于醛类 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
| 水中的溶解性 | 可溶于冷水 易溶于热水 | 可溶 | 易溶 | 易溶 |
| 乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |

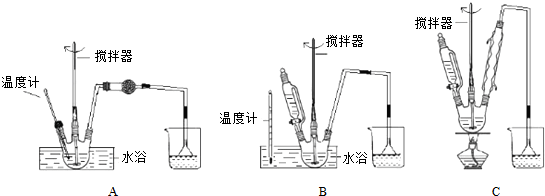
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com