
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | A | |||||||
| 二 | D | F | H | |||||
| 三 | B | C | E | G |
 ;化学性质最不活泼的是Ne,A与D形成的阳离子的电子式是
;化学性质最不活泼的是Ne,A与D形成的阳离子的电子式是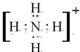 .
.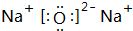 ,
, .其中B元素的原子与氧原子按1:1的个数比形成的化合物11.7g与足量二氧化碳完全反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2,有0.15mol 电子发生转移.
.其中B元素的原子与氧原子按1:1的个数比形成的化合物11.7g与足量二氧化碳完全反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2,有0.15mol 电子发生转移. 分析 根据元素在周期表中的位置知,A-H分别是H、Na、Al、N、P、F、Cl、Ne元素,
(1)元素的非金属性越强,其单质的氧化性越强,氟气分子中F原子之间存在一对共用电子对;
化学性质最不活泼的是稀有气体元素,A与D形成的阳离子是铵根离子,铵根离子之间N-H原子之间存在一对共用电子对;
(2)元素的金属性越强,其最高价氧化物的水化物碱性越强;元素的非金属性越强,其最高价氧化物的水化物酸性越强;
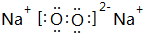
(3)Na元素可以形成两种氧化物,为氧化钠、过氧化钠;
其中B元素的原子与氧原子按1:1的个数比形成的化合物为Na2O2,过氧化钠和二氧化碳反应生成碳酸钠和氧气,n(Na2O2)=$\frac{11.7g}{78g/mol}$=0.15mol,该反应中氧化剂和还原剂都是过氧化钠,且有1mol过氧化钠完全反应就转移1mol电子.
解答 解:根据元素在周期表中的位置知,A-H分别是H、Na、Al、N、P、F、Cl、Ne元素,
(1)元素的非金属性越强,其单质的氧化性越强,非金属性最强的是F元素,则F2氧化性最强,氟气分子中F原子之间存在一对共用电子对,电子式为 ;
;
化学性质最不活泼的是稀有气体元素,为Ne,A与D形成的阳离子是铵根离子,铵根离子之间N-H原子之间存在一对共用电子对,电子式为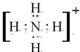 ;
;
故答案为:F2; ;Ne,
;Ne,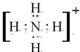 ;
;
(2)元素的金属性越强,其最高价氧化物的水化物碱性越强;元素的非金属性越强,其最高价氧化物的水化物酸性越强,金属性Na>Al、非金属性Cl>P,所以B、C、E、G四种元素的最高价氧化物对应水化物的化学式排列成序是NaOH Al(OH)3 H3PO4 HClO4,故答案为:NaOH Al(OH)3 H3PO4 HClO4;
(3)Na元素可以形成两种氧化物,为氧化钠、过氧化钠,电子式分别为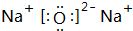 、
、 ;
;
其中B元素的原子与氧原子按1:1的个数比形成的化合物为Na2O2,过氧化钠和二氧化碳反应生成碳酸钠和氧气,反应方程式为2Na2O2+2CO2=2Na2CO3+O2,n(Na2O2)=$\frac{11.7g}{78g/mol}$=0.15mol,该反应中氧化剂和还原剂都是过氧化钠,且有1mol过氧化钠完全反应就转移1mol电子,所以有0.15mol过氧化钠完全反应转移0.15mol电子,
故答案为: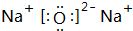 、
、 ;2Na2O2+2CO2=2Na2CO3+O2;0.15mol.
;2Na2O2+2CO2=2Na2CO3+O2;0.15mol.
点评 本题考查元素周期表结构和元素周期律综合应用,涉及电子式的书写、方程式的书写、化学方程式有关计算等知识点,难点是过氧化钠电子式的书写,为易错点.


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 该反应为可逆反应,故在一定条件下SO2和O2不可能全部转化为SO3 | |
| B. | 达到平衡后,反应就停止了,故正、逆反应速率相等且均为零 | |
| C. | 一定条件下,向某密闭容器中加入2 mol SO2和1 mol O2,则从反应开始到达到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻之后,正、逆反应速率相等 | |
| D. | 平衡时SO2、O2、SO3的分子数之比不再改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
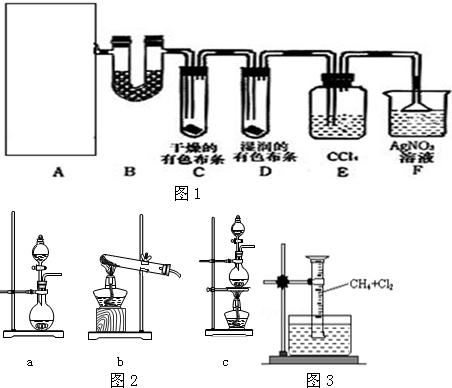
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
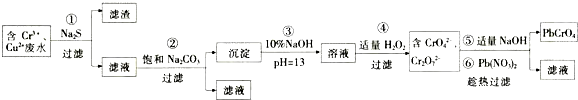
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族周期 | ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | VⅡA | 0 |
| 二 | ⑪ | ① | ② | |||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
 ;
; ;用电子式表示元素②与⑪化合物的形成过程
;用电子式表示元素②与⑪化合物的形成过程 ,该化合物属于共价(填“共价”或“离子”)化合物.
,该化合物属于共价(填“共价”或“离子”)化合物. ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
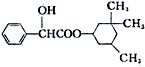 环扁桃酯具有松弛血管平滑肌、扩张血管的功能,其结构简式如图.下列对该物质的叙述中,正确的是( )
环扁桃酯具有松弛血管平滑肌、扩张血管的功能,其结构简式如图.下列对该物质的叙述中,正确的是( )| A. | 该物质属于芳香烃 | |
| B. | 该有机物不能被氧化成醛 | |
| C. | 分子式为C17H23O3 | |
| D. | 1mol该物质最多可与2 mol NaOH发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有达到平衡时,消耗O2的速率与生成NO的速率之比才为5;4 | |
| B. | 若单位时间生成xmolNO的同时,消耗xmolNH3,则反应达到平衡状态 | |
| C. | 达到平衡状态后,NH3、O2、NO、H2O(g)的物质的量保持不变 | |
| D. | 达到平衡状态时,若增加容器体积,则反应速率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com