
| A、等于20mL |
| B、小于20mL |
| C、等于30mL |
| D、大于30ml. |
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案科目:高中化学 来源: 题型:
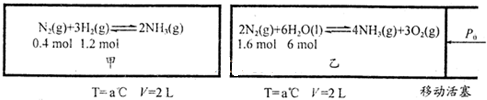
查看答案和解析>>
科目:高中化学 来源: 题型:
A、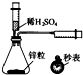 测定一定时间内生成H2的反应速率 |
B、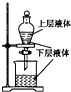 提取海带中的碘 |
C、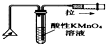 检验火柴燃烧产生的SO2 |
D、 证明非金属性:Cl>C>Si |
查看答案和解析>>
科目:高中化学 来源: 题型:
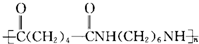 ,
,| A、HOOCCH2CH2CH2CH2CH2CH2COOH和H2NCH2CH2CH2CH2CH2CH2NH2 |
| B、HOOCCH2CH2CH2CH2CH2CH2COOH和H2NCH2CH2CH2CH2NH2 |
| C、HOOCCH2CH2CH2CH2CH2CH2NH2 |
| D、HOOCCH2CH2CH2CH2COOH和H2NCH2CH2CH2CH2CH2CH2NH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
物质 T/℃n/mol | 活性炭 | NO | E | F |
| 初始 | 2.030 | 0.10 | 0 | 0 |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
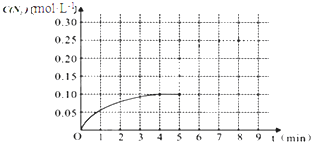
查看答案和解析>>
科目:高中化学 来源: 题型:
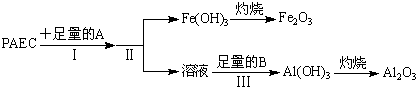
| 过量稀盐酸 |
| 试剂X |
| HCl(或NaOH) |
| 调节pH |
| 水解 |
| 聚合 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com