���
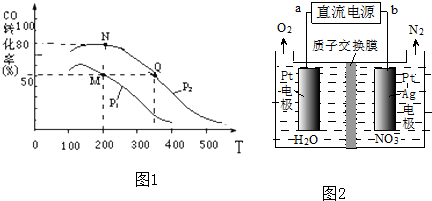
�⣺��1��ѹǿ����ʱ�������¶ȣ�COת���ʽ��ͣ�˵������Ӧ�Ƿ��ȷ�Ӧ���¶Ȳ���ʱ������ѹǿ��ƽ��������Ӧ�����ƶ�����COת����������ͼ��֪P2��P1��
��a�� ���۸÷�Ӧ�Ƿ�ﵽƽ��״̬������CH
3OH������������CO������ʼ����ȣ����Բ��ܾݴ��ж�ƽ��״̬���ʴ���
b�������������䡢����������䣬���Ի�������ܶ�ʼ�ղ��䣬���Բ��ܾݴ��ж��Ƿ�ﵽƽ��״̬���ʴ���
c����Ӧǰ����������ʵ����ı䣬������ƽ��Ħ�������ı䣬����Ӧ�ﵽƽ��״̬ʱ�������������ƽ�������������䣬�����ܾݴ��ж��Ƿ�ﵽƽ��״̬������ȷ��
d�� CH
3OH��CO��H
2��Ũ�ȶ����ٷ����仯ʱ�÷�Ӧ�ﵽƽ��״̬������ȷ��
��ѡcd��
��a������ƽ�����淴Ӧ�����ƶ�����COת���ʣ��ʴ���
b�����������Ӱ��ƽ���ƶ�����COת���ʲ��䣬�ʴ���
c������CO��Ũ��ƽ��������Ӧ�����ƶ�����COת���ʽ��ͣ��ʴ���
d������H
2��ѹ��ƽ��������Ӧ�����ƶ���COת����������ȷ��
e��������������ѹ��CO�������ͼ״�Ũ�Ȳ��䣬ƽ�ⲻ�ƶ����ʴ���
f��������״���ƽ��������Ӧ�����ƶ���COת����������ȷ��
��ѡdf��
��M��ʱ��COת����Ϊ50%����μӷ�Ӧ��n��CO��=10mol��50%=5mol����ʣ��5molCO�����ݷ���ʽ֪����ʣ��n��H
2��=20mol-5mol��2=10mol������n��CH
3OH��=5mol��N��ʱ��COת����Ϊ80%���μӷ�Ӧ��n��CO��=10mol��80%=8mol����ʣ��2molCO�����ݷ���ʽ֪����ʣ��n��H
2��=20mol-8mol��2=4mol������n��CH
3OH��=8mol�����������������ʵ����ʵ���֮��Ϊ��n��M��
����n��N��
��=��5+10+5��mol����2+4+8��mol=10��7��
��ͬ�¶��£���ѧƽ�ⳣ����ȣ���M���������ΪaL��N���������ΪbL��
M��ʱC��CO��=
mol/L��C��H
2��=
mol/L��n��CH
3OH��=
mol/L��
N��ʱC��CO��=
mol/L��C��H
2��=
mol/L��n��CH
3OH��=
mol/L��
���ݻ�ѧƽ�ⳣ����ȵ�
=
��a��b=5��1
�ʴ�Ϊ��10��7��5��1��
�ܻ�ѧƽ�ⳣ��ֻ���¶��йأ���ͬ�¶�ʱ��ƽ�ⳣ����ȣ������¶�ƽ�����淴Ӧ�����ƶ�����ƽ�ⳣ����С������ͼ��֪���¶ȣ�M=N��Q������M��N��Q�����ƽ�ⳣ��K
M��K
N��K
Q�Ĵ�С��ϵΪK
M=K
N��K
Q���ʴ�Ϊ��K
M=K
N��K
Q��
��2������H
2��NO
3-��ԭΪN
2��һ��ʱ�����Һ�ļ���������ǿ��˵���÷�Ӧ���������������ӣ�ͬʱ������ˮ�����Է�Ӧ����ʽΪ2NO
3-+5H
2N
2+2OH
-+4H
2O���ʴ�Ϊ��2NO
3-+5H
2N
2+2OH
-+4H
2O��
�ڸ���ͼ��֪����������ӵõ��ӷ�����ԭ��Ӧ����bΪ������aΪ���������ݵ�ط�Ӧʽ֪����������������ӵõ������ɵ�����ˮ���缫��ӦʽΪ2NO
3-+12H
++10e
-=N
2+6H
2O���ʴ�Ϊ��a��2NO
3-+12H
++10e
-=N
2+6H
2O��




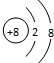


 ʵ������Ҫ����0.1mol?L-1 CuSO4��Һ480mL��
ʵ������Ҫ����0.1mol?L-1 CuSO4��Һ480mL��