
| A. | Cl-、SO42-、Mg2+、Al3+ | B. | Na+、K+、Cl-、SO42- | ||
| C. | Na+、K+、Cl-、CO32- | D. | Na+、Fe3+、Cl-、HCO3- |
分析 溶液无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,与铝反应生成氢气的溶液为酸性或强碱性溶液,
A.镁离子、铝离子与碱性溶液中的氢氧根离子反应;
B.四种离子之间不反应,都是无色离子,都不与氢离子和氢氧根离子反应;
C.碳酸根离子与氢离子反应;
D.铁离子为有色离子,且铁离子与碳酸氢根离子发生双水解反应.
解答 解:无色溶液可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,与铝反应生成氢气的溶液为酸性或强碱性溶液,溶液中存在大量氢离子或氢氧根离子,
A.Mg2+、Al3+与氢氧根离子反应,在碱性溶液中不能大量共存,故A错误;
B.Na+、K+、Cl-、SO42-之间不反应,都不与氢离子和氢氧根离子反应,且为无色溶液,在溶液中能够大量共存,故B正确;
C.CO32-与酸性溶液中的氢离子反应,在酸性溶液中不能大量共存,故C错误;
D.Fe3+、HCO3-之间发生双水解反应,且Fe3+为有色离子,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间等;解决离子共存问题时还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;溶液的具体反应条件,如“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,16g14CH4所含中子数目为8NA | |
| B. | 标准状况下,7.8g苯中含碳碳双键的数目为0.3 NA | |
| C. | 含0.2NA个阴离子的Na2O2和水完全反应转移0.2mol电子 | |
| D. | 0.1L 3mol•L-1的NH4NO3溶液中含有的NH4+数目为0.3N |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蛋白质、纤维素、油脂、PVC塑料、淀粉都是高分子化合物 | |
| B. | 麦芽糖与蔗糖的水解产物均含葡萄糖,故二者均为还原性二糖 | |
| C. | 若两种二肽互为同分异构体,则二者的水解产物不一致 | |
| D. | 甲醛、氯乙烯和乙二醇均可作为合成聚合物的单体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定温度下的可逆反应,只有达到平衡时才具有平衡常数 | |
| B. | 化学平衡移动时,平衡常数一定改变 | |
| C. | 对于一个确定的反应来说,平衡常数的数值越大,反应限度越大 | |
| D. | 化学平衡常数大的可逆反应,所有反应物的转化率一定大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 太阳能热水器、反射式太阳灶 | |
| B. | 太阳能电池 | |
| C. | 利用生活垃圾中生物质能焚烧发电 | |
| D. | 通过植物的光合作用,产生生物质能 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 元素 | 原子结构特征或有关物质的性质 |
| A | 原子的最外层电子数是其内层电子数的2倍 |
| B | 其单质是空气中含量最多的物质 |
| C | 原子的最外层电子数是其电子层数的4倍 |
| D | 位于第ⅡA族,其原子半径比E的大 |
| E | 是金属元素,其氧化物和氢氧化物都有两性,且与D在同一周期 |
| F | 原子序数16,其单质在通常状况下为固体 |
| G | 原子的最外层电子数比其次外层电子数少1个 |
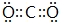 .
. NH4++OH-(用方程式表示)
NH4++OH-(用方程式表示)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com