
| A. | 26Fe的价层电子排布式为3d64s2 | |
| B. | 35Br的电子排布式可简写为[Ar]4s24p5 | |
| C. | NH4Cl的电子式为  | |
| D. | 氯离子结构示意图为 |
分析 A、26Fe的价层电子为最外层加上次外层d能级上的电子;
B、35Br的电子排布式为1s22s22p63s23p63d104s24p5;
C、NH4Cl的电子式中氯离子没有标出最外层电子;
D、Cl-的最外层电子数为8,核外电子总数为18.
解答 解:A、26Fe的价层电子为最外层加上次外层d能级上的电子,所以价层电子为排布式为3d64s2,故A正确;
B、35Br的电子排布式为1s22s22p63s23p63d104s24p5,则35Br的电子排布式可简写为[Ar]3d104s24p5,故B错误;
C、NH4Cl为离子化合物,阴阳离子需要标出所带电荷,铵根离子和氯离子还应该标出最外层电子,氯化铵正确的电子式为 ,故C错误;
,故C错误;
D、Cl-的结构示意图中,最外层电子数为8,氯离子正确的结构示意图为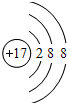 ,故D错误;
,故D错误;
故选:A.
点评 本题考查了核外电子排布、电子式、结构示意图的判断,题目难度中等,注意掌握常见的化学用语的概念及正确表示方法,试题培养了学生灵活应用所学知识的能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
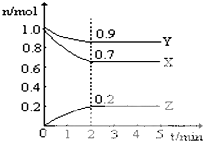 某温度时,在一个10L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:
某温度时,在一个10L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③② | C. | ④② | D. | ③① |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 碳及其化合物与人类关系密切
碳及其化合物与人类关系密切 ,C、N、O三元素的第一电离能由大到小的顺序为N>O>C,在丙烯分子中碳原子的杂化方式为sp2、sp3.
,C、N、O三元素的第一电离能由大到小的顺序为N>O>C,在丙烯分子中碳原子的杂化方式为sp2、sp3.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
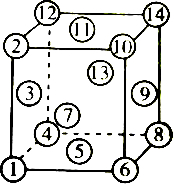
| A. | ④⑤⑥⑩⑪⑫ | B. | ②③④⑤⑥⑦ | C. | ①④⑤⑥⑧ | D. | ①②⑪⑭⑧⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝原子核外有13种不同运动状态的电子 | |
| B. | 前四周期元素中,基态原子中成对电子数与其所在周期数相同的元素有6种 | |
| C. | 第一电离能介于B、N之间的第二周期元素有3种 | |
| D. | HF的水溶液中存在4种氢键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 气态氢化物稳定性:R>Q | |
| B. | 元素T的离子结构示意图为 | |
| C. | 与w同主族的某元素形成的18电子的氢化物分子中只有共价键没有离子键 | |
| D. | Q可形成多种含氧酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com