
【题目】下列药品属于国际奥委会严格禁止的兴奋剂是
A. 阿司匹林 B. 青霉素 C. 麻黄碱 D. 氢氧化铝
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】合成药物X、Y 和高聚物Z,可以用烃A为主要原料,采用以下路线。
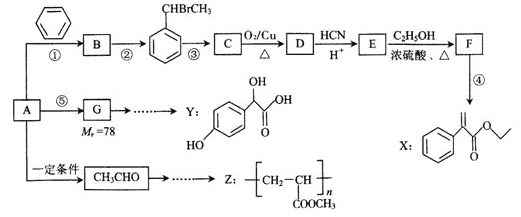
已知I.反应①、反应②的原子利用率均为100%。
II.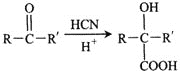 (R或R′可以是烃基或H原子)
(R或R′可以是烃基或H原子)
请回答下列问题:
(1)A的结构简式为________________。
(2)Z中的官能团名称为_____________________,反应③的条件为_________________。
(3) 关于药物Y(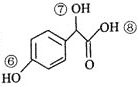 )的说法正确的是_____________________。
)的说法正确的是_____________________。
A.1mol 药物Y与足量的钠反应可以生成33.6L氢气
B.药物Y 的分子式为C8H8O4,能使酸性高锰酸钾溶液褪色
C.药物Y 中⑥、⑦、⑧三处-OH 的活泼性中强到弱的顺序是⑧>⑥>⑦
D.1mol药物Y与H2、浓溴水中的Br2反应,最多消耗分别为4mol和2mol
(4)写出反应E→F 的化学方程式________________。F→X的化学方程式_________________。
(5)写出符合下列条件的E的一种同分异构体的结构简式_________________________。
①FeCl3溶液可以发生显色反应,且是苯的二元取代物;
②能发生银镜反应和水解反应;
③核磁共振氢谱有6个峰。
(6)参考上述流程以CH3CHO和CH3OH为起始原料,其它无机试剂任选设计合成Z 的线路。__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有如下两个反应:a.NaOH+HCl=NaCl+H2O b.Cu+2Ag+ =Cu2+ +2Ag
(1)反应____(填字母)不能设计成原电池。原因是__________________________。
(2)a反应为______反应(填“放热”或“吸热”),NaOH和HCl的总能量________(填“大于”“小于”或“等于”)NaCl和H2O的总能量。
(3)已知HCl中H-Cl键的键能为431 kJ·mol-1,则断开1molH-Cl键_____431 kJ的能量,形成1molH-Cl键_____431 kJ的能量。(填“吸收”或“放出”)
(4)反应____(填字母)能设计成原电池,请画出实验装置图,注明电极材料和电解质溶液。__________

写出电极反应式及反应类型
正极反应式:_____________________,
反应类型:_______________________,
负极反应式:_____________________。
(5)上题所设计原电池中,向正极移动的离子为_______,电池工作一段时间后,电解质溶液质量减轻7.6g,正极增重的质量为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近几年来关于氮污染的治理倍受关注。
(1)三效催化剂是最为常见的汽车尾气催化剂,能同时实现汽车尾气中的CO、CxHy、NOx三种成分的净化,其催化剂表面物质转化的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定。
图1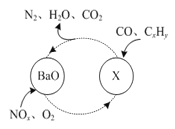 图2
图2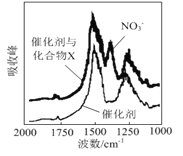
①在图示的转化中,被还原的元素是_______________,X的化学式为________________。
②钡元素在周期表中的位置是_________________。
(2)SCR技术可使NOx与NH3直接反应,实现无害转化。当NO与NO2的物质的量之比为2:1时,写出发生反应的化学方程式:___________________。
(3)利用ClO2 氧化氮氧化物反应过程如下:NO![]() NO2
NO2![]() N2
N2
反应Ⅰ的化学方程式是2NO + ClO2 + H2O == NO2 + HNO3 + 2HCl,反应Ⅱ的离子方程式是______________。
(4)加入过量次氯酸钠可使废水中NH4+ 完全转化为N2,而本身被还原为NaCl。
①写出次氯酸钠的电子式_________________。
②检验废水中是否存在NH4+的方法是____________________________。
③若处理废水产生了0.448LN2(标准状况),则需消耗浓度为2mol·L-1的次氯酸钠的体积为_______________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中充入CO和CO2的混合气体,其密度是相同条件下氦气密度的8倍,这时测得容器内压强为P1,若控制容器的体积不变,加入足量的过氧化钠,并不断用电火花点燃至完全反应,恢复到开始的温度,再次测得容器内的压强为P2,则P1和P2关系是
A. P1=8P2 B. P1=4P2 C. P1=2P2 D. P1=P2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】格氏试剂在有机合成方面用途广泛,可用卤代烃和镁在醚类溶剂中反应制得。设R为烃基,已知:
①RX +Mg![]() R-MgX(格氏试剂);
R-MgX(格氏试剂);
②
阅读以下合成路线图,回答有关问题:
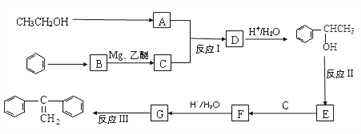
(1)反应I的类型是_____________,反应II的条件是___________________ 。
(2)反应III的化学方程式为____________________________________ 。
(3)E的同分异构体中,含有苯环且能发生银镜反应的有机物共有____种。
(4)有机物 ![]() 是合成药物中的一种原料,实验室可用下列合成路线合成该有机物:
是合成药物中的一种原料,实验室可用下列合成路线合成该有机物:
其中Z的结构简式为________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜板上铁铆钉长期暴露在潮湿的空气中,形成一层酸性水膜后铁铆钉会被腐蚀,示意图如下。下列说法不正确的是
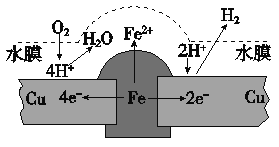
A. 因铁的金属性比铜强,所以铁铆钉被氧化而腐蚀
B. 若水膜中溶解了SO2,则铁铆钉腐蚀的速率变小
C. 铜极上的反应是2H+ + 2e- = H2↑,O2 + 4e-+ 4H+ = 2H2O
D. 在金属表面涂一层油脂,能防止铁铆钉被腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X和Y两元素组成化合物A和B,A的化学式为XY2,其中X占44.1%,B中X占34.5%,则B的化学式为( )
A.X2YB.XYC.XY3D.X3Y
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com