
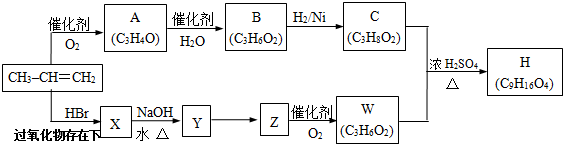
| 水 |
| △ |
| 水 |
| △ |
| △ |
| △ |
| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
| B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C、蒸发结晶时应将溶液蒸干 |
| D、用固体NaOH配制一定物质的量浓度的NaOH溶液时,NaOH溶于水后,应冷却至室温才能转移到容量瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:

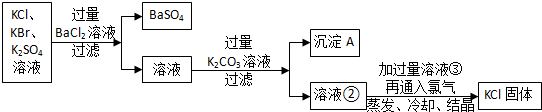
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO2和NO |
| B、CO2 |
| C、NO |
| D、NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、N2(g)+3H2(g)?2NH5(g)△H=-Q1kJ?mol-1(Q1>0) |
| B、2SO5(g)?2SO2(g)+O2(g)△H=+Q2kJ?mol-1(Q2>0) |
| C、4NH5(g)+5O2(g)?4NO(g)+6H2O(g)△H=-Q3kJ?mol-1(Q3>0) |
| D、H2(g)+CO(g)?C(g)+H2O(g)△H=+Q4kJ?mol-1(Q4>0) |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 “白铁皮”即镀锌铁皮,镀锌层犹如铁皮的保护层,具有较强的耐腐蚀性,这层膜的厚度是判断白铁皮质量的重要指标,某研究性学习小组为了测定镀膜厚度,设计了下面的实验方案.
“白铁皮”即镀锌铁皮,镀锌层犹如铁皮的保护层,具有较强的耐腐蚀性,这层膜的厚度是判断白铁皮质量的重要指标,某研究性学习小组为了测定镀膜厚度,设计了下面的实验方案.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3OH |
| B、C2H5OH |
| C、C3H7OH |
| D、C4H9OH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com