
【题目】把3.06 g铝和镁的混合物粉末放入100 mL盐酸中,恰好完全反应,并得到标准状况下3.36 LH2 计算:(要有过程)
(1)该合金中铝的物质的量_____。
(2)反应后溶液中Cl﹣的物质的量浓度(假定反应体积仍为100 mL)____。
【答案】0.06 mol 3.0 mol·L-1
【解析】
(1)根据n=![]() 计算出生成氢气的物质的量,设出铝和镁的物质的量,分别根据质量和生成氢气的量列式计算;
计算出生成氢气的物质的量,设出铝和镁的物质的量,分别根据质量和生成氢气的量列式计算;
(2)反应后溶质为氯化镁和氯化铝,根据质量守恒计算出氯离子的物质的量,再根据c=![]() 计算出氯离子的浓度。
计算出氯离子的浓度。
(1)标准状况下3.36L氢气的物质的量为:![]() =0.15mol,设3.06g金属的混合物中含有Al和Mg的物质的量分别为x、y,则:27x+24y=3.06、
=0.15mol,设3.06g金属的混合物中含有Al和Mg的物质的量分别为x、y,则:27x+24y=3.06、![]() x+y=0.15,解得:x=0.06mol、y=0.06mol,则该合金中铝的物质的量为0.06mol;
x+y=0.15,解得:x=0.06mol、y=0.06mol,则该合金中铝的物质的量为0.06mol;
(2)合金与盐酸恰好完全反应,反应后溶质为氯化铝和氯化镁,则反应后溶液中含有氯离子的总物质的量为:0.06mol×2+0.06mol×3=0.3mol,所以反应后溶液中氯离子的浓度为:![]() =3.0mol/L。
=3.0mol/L。


科目:高中化学 来源: 题型:
【题目】某喜温植物幼苗在低温锻炼(10 ℃、6天)后,接着进行冷胁迫(2℃、12 h),其细胞内超氧化物歧化酶 (SOD,该酶能减缓植株的衰老)活性的动态变化图如下。下列相关分析错误的是

A.该实验目的为探究低温锻炼是否能提高植物抗寒能力
B.未锻炼组冷胁迫后SOD活性降低是由于其空间结构发生了改变
C.无论是否锻炼胁迫后SOD降低化学反应活化能的能力均降低
D.低温锻炼能提高SOD活性且其在冷胁迫后SOD活性相对较稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌元素对婴儿及青少年的智力和身体发育有重要的作用,被称为生命火花。利用恒电势电解NaBr溶液间接将葡萄糖[CH2OH(CHOH)4CHO]氧化为葡萄糖酸[CH2OH(CHOH)4COOH],进而制取葡萄糖酸锌,装置如图所示,下列说法错误的是( )

A.钛网与直流电源的正极相连,发生还原反应
B.石墨电极的反应为2H2O+2e-=H2↑+2OH-
C.电解过程中硫酸钠溶液浓度保持不变
D.生成葡萄糖酸的化学方程式为CH2OH(CHOH)4CHO+Br2+H2O=CH2OH(CHOH)4COOH+2HBr
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,表中列出11种元素在周期表中的位置,按要求回答下列各题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ⑥ | ⑧ | ||||||
3 | ① | ③ | ⑤ | ⑦ | ⑨ | |||
4 | ② | ④ | ⑩ |
(1)这11种元素中,化学性质最不活泼的元素是______(填元素符号,下同),得电子能力最强的原子是______,失电子能力最强的单质与水反应的化学方程式__。
(2)元素④的离子结构示意图为___________。
(4)写出③的单质置换出⑥的单质的化学方程式:_____。
①和⑤两种元素最高价氧化物对应的水化物相互反应的离子方程式为________。
②的最高价氧化物对应水化物与⑤的最高价氧化物反应的化学方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锥形瓶内盛有气体X,滴管内盛有液体Y。若挤压胶头滴管,使液体Y滴入瓶中,振荡,过一会可见小气球a鼓起。气体X和液体Y不可能是( )
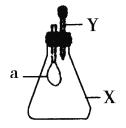
A.X是NH3,Y是水
B.X是SO2,Y是NaOH浓溶液
C.X是CO2,Y是稀硫酸
D.X是HCl,Y是NaNO3稀溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~H为中学化学中常见的物质,转化关系如下所示,其中“O”代表化合物,“□”代表单质,A为医疗上治疗胃酸过多的一种药剂,G为淡黄色固体,C在通常状况下为无色液体.

请回答下列问题:
(1)G的化学式为________,每生成1 mol G转移电子________mol.
(2)反应①②③④中________(填序号)属于氧化还原反应.
(3)写出下列反应的化学方程式:A→B+C+D:_______________________________,F+C:________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组探究SO2气体还原Fe3+、I2(体系均为酸性条件),它们使用的药品和装置如图所示:

(1)SO2气体还原Fe3+后的所有产物有___________(填离子符号),参加反应的SO2和Fe3+的物质的量之比是______________;
(2)写出装置B中反应的离子方程式________________________;装置C的作用是________________________。
(3)若要从A中所得溶液提取晶体,必须进行的实验操作步骤:蒸发、冷却结晶、过滤、然后干燥,在这一系列操作中没有用到的仪器是____________
A、蒸发皿 B、石棉网 C、漏斗 D、玻璃棒 E、坩埚
(4)在上述装置中通入过量的SO2,为了验证SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分为三份,并设计了如下实验:
方案①:往第一份试液中加入酸性KMnO4溶液,紫红色褪去;
方案②:往第二份试液中加入KSCN溶液(硫氰化钾,遇到Fe3+时溶液变成血红色),溶液不变红,再加入某种氧化剂,溶液变红;
方案③:往第三份试液中加入用盐酸酸化的BaCl2溶液,产生白色沉淀。
上述方案不合理的是_______________,原因是___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。

请到答F列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是 ,其中发生反应的化学方程式为 ;
(2)实验过程中,装置B、C中发生的现象分别是 、 ,这些现象分别说明SO2具有的性质是 和 ;装置B中发生反应的离子方程式为 ;
(3)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象 ;
(4)尾气可采用 溶液吸收。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 标准状况下,22.4 L水含有的水分子数为NA
B. 常温常压下,22 g CO2含有的CO2分子数为0.5NA
C. 标准状况下,32 g O2和CO2的混合气体含有的氧原子数为2NA
D. 40 g NaOH溶解在1 L水中,得到溶液的物质的量浓度为1 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com