
如图所示,某同学做乙醇氧化实验时,将螺旋状铜丝先放到a点处加热,然后再移到b点,发现铜丝在火焰a、b两点现象明显不同。请你写出a、b两点的实验现象,并解释产生该现象的原因。

|
|
实验现象 |
解释 |
化学方程式 |
|
a |
|
|
|
|
b |
|
|
|
a.铜丝变黑 外焰处乙醇充分燃烧,铜丝被氧化 2Cu+O2 2CuO
2CuO
b.铜丝又变回红色 焰芯处乙醇未充分燃烧,使氧化铜被还原 CH3CH2OH+CuO CH3CHO+H2O+Cu
CH3CHO+H2O+Cu
【解析】
试题分析:本题考查乙醇发生氧化反应的条件及在不同条件下的不同产物。解决这类题目,关键是弄清乙醇燃烧反应和催化氧化反应。①燃烧:CH3CH2OH+3O2 2CO2+3H2O。②催化氧化:2CH3CH2OH+O2
2CO2+3H2O。②催化氧化:2CH3CH2OH+O2 2CH3CHO+2H2O。a点乙醇充分燃烧,生成二氧化碳和水,并放热,使铜丝被氧气氧化。b点由于氧气不足,有乙醇蒸气未完全燃烧,使前面生成的氧化铜还原成铜,CH3CH2OH+CuO
2CH3CHO+2H2O。a点乙醇充分燃烧,生成二氧化碳和水,并放热,使铜丝被氧气氧化。b点由于氧气不足,有乙醇蒸气未完全燃烧,使前面生成的氧化铜还原成铜,CH3CH2OH+CuO CH3CHO+H2O+Cu。
CH3CHO+H2O+Cu。
考点:考查乙醇催化氧化实验的探究
点评:该题以乙醇的催化氧化实验探究为载体,,重点考查学生的实验分析、设计、观察以及动手操作能力,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于调到学生的学习积极性,提高学生的应试能力。


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:阅读理解
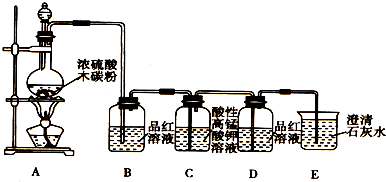
 某研究性学习小组的同学决定通过实验探究SO2的漂白性是SO2本身具有的还是SO2与水作用的产物具有的,他们查阅资料知品红能溶解在酒精中形成红色溶液.
某研究性学习小组的同学决定通过实验探究SO2的漂白性是SO2本身具有的还是SO2与水作用的产物具有的,他们查阅资料知品红能溶解在酒精中形成红色溶液.- 3 |
2- 3 |
- 3 |
2- 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 氯化铁溶液用量 | 10滴 | 20滴 | 30滴 | 2mL | 3mL | 4mL |
| 萃取后上层溶液颜色 | 黄色 | 黄色 | 黄色 | 较深黄色 | 黄色略带红色 | 黄红色 |
| 加入KSCN溶液后颜色 | 不变红 | 不变红 | 略变红 | 偏血红色 | 血红色 | 血红色 |
| c(I-)/mol?L-1 | c(Fe3+)/mol?L-1 | v/mol?L-1?s-1 | |
| ① | 0.20 | 0.80 | 0.032k |
| ② | 0.60 | 0.40 | 0.144k |
| ③ | 0.80 | 0.20 | 0.128k |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年湖北省荆州市高三毕业班质量检查(Ⅰ)化学试卷(解析版) 题型:填空题
如下图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。请按要求回答相关问题:
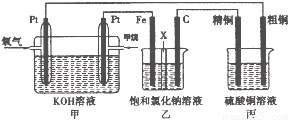
(1)甲烷燃料电池负极电极反应式是:
(2)石墨电极(C)的电极反应式为
(3)若在标准状况下,有2. 24 L氧气参加反应,则乙装置中铁电极上生成的气体体积为_ L;丙装置中阴极析出铜的质量为 g
(4)某同学利甲烷燃料电池设计电解法制取漂白液或Fe(OH)2的实验装置(如图所示)。若用于制漂白液时a为电池_ 极,电解质溶液最好用_ 。若用于制 Fe(OH)2,使用硫酸钠做电解质溶液,阳极选用 作电极。

查看答案和解析>>
科目:高中化学 来源:专项题 题型:单选题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com