
 .
.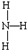 .X在纯氧中燃烧的产物无毒无污染,该反应的化学方程式为4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O.
.X在纯氧中燃烧的产物无毒无污染,该反应的化学方程式为4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O. .
.分析 A、B、C、D、E、F六种短周期主族元素,原子序数依次增大,其中B的单质在常温下为双原子分子,它与A的单质可形成分子X,X的水溶液呈碱性,所以X为NH3,A的原子序数比B小,则B为N元素,A为H元素;D的简单阳离子与X具有相同电子数,NH3含有10个电子,D的简单阳离子为10e-结构,且D是同周期中原子半径最大的元素,则D为Na元素;E元素的原子最外层比次外层少两个电子,E的原子序数大于Al,则E有3个电子层,最外层电子数为6,则E为S元素;F的原子序数比E大且为短周期主族元素,则F是Cl元素;C、F两种元素的原子最外层共有13个电子,C最外层有6个电子,原子序数比Na小,则C为O元素,结合元素对应的单质、化合物的性质解答该题.
解答 解:A、B、C、D、E、F六种短周期主族元素,原子序数依次增大,其中B的单质在常温下为双原子分子,它与A的单质可形成分子X,X的水溶液呈碱性,所以X为NH3,A的原子序数比B小,则B为N元素,A为H元素;D的简单阳离子与X具有相同电子数,NH3含有10个电子,D的简单阳离子为10e-结构,且D是同周期中原子半径最大的元素,则D为Na元素;E元素的原子最外层比次外层少两个电子,E的原子序数大于Al,则E有3个电子层,最外层电子数为6,则E为S元素;F的原子序数比E大且为短周期主族元素,则F是Cl元素;C、F两种元素的原子最外层共有13个电子,C最外层有6个电子,原子序数比Na小,则C为O元素,
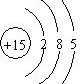
(1)B为N元素,与B同主族的元素为P,原子结构示意图为 ,
,
故答案为: ;
;
(2)X为氨,结构式为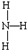 ,氨在纯氧中反应生成氮气和水,方程式为4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O,
,氨在纯氧中反应生成氮气和水,方程式为4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O,
故答案为: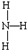 ;4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O;
;4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O;
(3)C与D可形成两种化合物甲和乙,为过氧化钠和氧化钠,过氧化钠与水反应的离子方程式为2Na2O2+2H2O=4Na++4OH-+O2↑,根据方程式知,标准状况下每生成5.6L气体,电子转移数目为0.5NA,Na2O为离子化合物,用电子式表示Na2O的形成过程为 ,
,
故答案为2Na2O2+2H2O=4Na++4OH-+O2↑;0.5NA; ;
;
(4)C、D、F形成的简单离子分别为O2-、Na+、Cl-,电子层数越多半径越大,相同电子层数,原子序数越大半径越小,半径由小到大的顺序为 Na+<O2-<Cl-,
故答案为:Na+<O2-<Cl-;
(5)最外层电子数与F相同,最高化合价却不同的元素,其单质为氟气,与水反应的化学方程式为 2F2+2H2O=4HF+O2,
故答案为:2F2+2H2O=4HF+O2.
点评 本题考查结构性质位置关系的应用,难度不大,推断元素是解题关键,“X的水溶液呈碱性”是推断突破口,注意电子式表示物质形成过程的书写,左边为原子电子式,右边为物质的电子式,中间用箭头连接.


科目:高中化学 来源: 题型:填空题
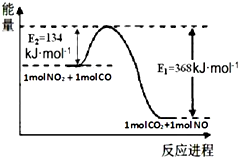 己知1mol NO2和1mol CO反应生成CO2和NO过程中能量变化如图所示.请写出NO2和CO反应的热化学方程式NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ•mol-1.
己知1mol NO2和1mol CO反应生成CO2和NO过程中能量变化如图所示.请写出NO2和CO反应的热化学方程式NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ•mol-1.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
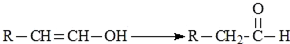
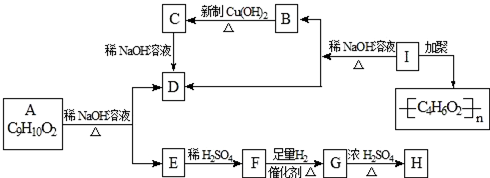
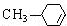 ,H:CH3COOCH=CH2.
,H:CH3COOCH=CH2.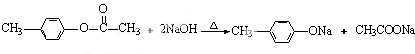 +H2O.
+H2O. ,
, .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
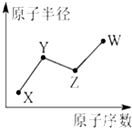 U、V、W、X、Y、Z是六种常见的短周期主族元素,其中W、X、Y、Z原子半径随
U、V、W、X、Y、Z是六种常见的短周期主族元素,其中W、X、Y、Z原子半径随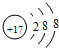 ;
;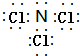 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 石墨燃烧热为-393.5kJ/mol | |
| B. | CO2和金刚石(或石墨)反应生成CO为吸热反应 | |
| C. | 等量金刚石和石墨完全燃烧,石墨放出的热量更多 | |
| D. | 12g石墨在一定量空气中燃烧,生成气体36g,该过程放出的热量为252.0kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式为:CH2CH2 | B. | 溴乙烷的分子式为:C2H5Br | ||
| C. | 丙烷分子的比例模型为: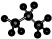 | D. | 四氯化碳分子的电子式为: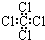 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向2%的稀氨水中滴入2%的硝酸银溶液至沉淀恰好溶解,配得银氨溶液 | |
| B. | 实验前试管先用热的烧碱溶液洗涤,再用蒸馏水洗涤 | |
| C. | 醛类一定能发生银镜反应,能发生银镜反应的一定是醛类 | |
| D. | 可用浓盐酸洗去银镜 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
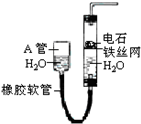 如图中的实验装置,可用于制取乙炔,请填写下列空白:
如图中的实验装置,可用于制取乙炔,请填写下列空白: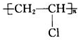 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com