
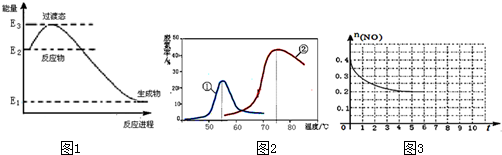
分析 (1)根据能量变化图,反应热=正反应的活化能-逆反应的活化能,再根据热化学反应方程式的书写解答;
(2)当正逆反应速率不相等时,化学平衡会向着正方向或是逆方向进行;
(3)反应自发进行的判断依据是△H-T△S<0;
(4)A.催化剂只影响反应速率,不会改变转化率;
B.增大压强平衡向逆反应方向移动;
C.最高点为催化剂活性最高的温度;
D.根据图象判断,脱氨率最高的点对应的温度应是最适宜温度;
(5)已知反应为2NO(g)+2CO(g)?N2(g)+2CO2(g),2L密闭容器中充入NO、CO各0.4mol,达到平衡时NO为0.2mol,利用三段式求出平衡浓度,再根据K=$\frac{c({N}_{2}){c}^{2}(C{O}_{2})}{{c}^{2}(NO){c}^{2}(CO)}$计算;第6分钟继续加入0.2molNO、0.2molCO、0.2molCO2和0.3molN2,根据Qc=$\frac{c({N}_{2}){c}^{2}(C{O}_{2})}{{c}^{2}(NO){c}^{2}(CO)}$计算,然后比较Qc与K的大小关系判断移动方向,再作图;
(6)氮的氧化物具有氧化性,要把NOx脱氮转化成无毒的N2,需要加还原剂,据此分析.
解答 解:(1)一定条件下H2还原NO生成N2和1mol水蒸气,依据能量变化图可知反应放热,反应焓变△H=E1-E2,反应的热化学方程式为:2H2(g)+2NO(g)=N2(g)+2H2O (g)△H=2(E1-E2)kJ•mol-1,
故答案为:2H2(g)+2NO(g)=N2(g)+2H2O (g)△H=2(E1-E2)kJ•mol-1;
(2)化学平衡的标志是正逆反应速率相等,当逆反应速率大于正反应速率时,说明反应是逆向进行的,CO(g)+2H2(g)?CH3OH(g)△H<0;
A.正反应速率先增大后减小,说明反应正向进行,故A正确;
B.逆反应速率先增大后减小,说明反应逆向进行,故B错误;
C.化学平衡常数K值增大,说明平衡正向进行,故C正确;
D.反应物的体积百分含量增大,可能逆向进行,也可能正向进行,不能说明反应正向进行,故D错误;
E.恒容容器中加入生成物,平衡逆向进行,气体质量增大,条件不变,混合气体的密度增大,故E错误;
F.平衡逆向进行氢气的转化率减小,故F错误;
故答案为:AC;
(3)2NO(g)+2CO(g)?N2(g)+2CO2(g)△H<0,反应前后气体体积减小△S<0,低温下满足△H-T△S<0,即在低温时反应自发进行,
故答案为:低温;
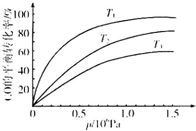
(4)A.催化剂不会影响转化率,只影响反应速率,所以第②种催化剂和第①种催化剂对转化率没有影响,故A错误;
B.反应为体积增大的反应,增大压强平衡向逆反应方向移动,脱氮率减小,故B错误.
C.图象研究的是不同催化剂在不同的温度下的活性比较,最高点为催化剂活性最大的状态,与平衡转化率无关,故C错误;
D.两种催化剂分别在55℃和75℃左右催化效率最高,说明此时催化剂的活性最大,故D正确;
故选D.
故答案为:D;
(5)已知反应为2NO(g)+2CO(g)?N2(g)+2CO2(g),2L密闭容器中充入NO、CO各0.4mol,达到平衡时NO为0.2mol,
2NO(g)+2CO(g)?N2(g)+2CO2(g)
起始(mol):0.4 0.4 0 0
转化(mol):0.2 0.2 0.1 0.2
平衡(mol):0.2 0.2 0.1 0.20.2
则K=$\frac{c({N}_{2}){c}^{2}(C{O}_{2})}{{c}^{2}(NO){c}^{2}(CO)}$=$\frac{(\frac{0.2}{2})^{2}×\frac{0.1}{2}}{(\frac{0.2}{2})^{2}×(\frac{0.2}{2})^{2}}$=5;
第6分钟继续加入0.2molNO、0.2molCO、0.2molCO2和0.3molN2,则c(NO)=$\frac{0.2mol+0.2mol}{2L}$=0.2mol/L,c(CO)=$\frac{0.2mol+0.2mol}{2L}$=0.2mol/L,
c(N2)=$\frac{0.1mol+0.3mol}{2L}$=0.2mol/L,c(CO2)=$\frac{0.2mol+0.2mol}{2L}$=0.2mol/L,
Qc=$\frac{c({N}_{2}){c}^{2}(C{O}_{2})}{{c}^{2}(NO){c}^{2}(CO)}$=$\frac{0.2×0.{2}^{2}}{0.{2}^{2}×0.{2}^{2}}$=5=K,说明是平衡状态,所以第6分钟继续加入0.2molNO、0.2molCO、0.2molCO2和0.3molN2,仍是平衡状态,但是NO的物质的量变为原来的2倍,作图为 ;
;
故答案为:5; ;
;
(6)氮的氧化物具有氧化性,要把NOx脱氮转化成无毒的N2,需要加还原剂,NH3、CH4、尿素均可作还原剂,KMnO4是常用的氧化剂,所以ABD正确;
故答案为:ABD.
点评 本题考查化学反应速率与化学平衡移动问题,化学平衡常数及影响因素、意义,反应速率计算等,难度中等,本题注意分析图象曲线的变化趋势,侧重于考查学生的读图能力和分析能力.


 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源: 题型:选择题
| A. | 46g乙醇中存在的共价键总数为7NA | |
| B. | 1mol甲醇完全燃烧时,转移的电子数为6NA | |
| C. | 标准状况下,22.4L甲烷和22.4L氯仿所具有的微粒数均为NA | |
| D. | 1 L 0.1mol/L醋酸溶液中含有的氢离子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 铁及其化合物在日常生活、生产中应用广泛,研究铁及其化合物的应用意义重大.回答下列问题:
铁及其化合物在日常生活、生产中应用广泛,研究铁及其化合物的应用意义重大.回答下列问题:| 温度 | 250℃ | 600℃ | 1000℃ | 2000℃ |
| 主要成分 | Fe2O3 | Fe3O4 | FeO | Fe |
| t/min | 0 | 10 | 20 | 30 | 40 | 50 |
| x(CO) | 0.25 | 0.23 | 0.214 | 0.202 | 0.193 | 0.193 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物理性质 | 制备原理 | 化学性质 |
| 黄色油状液体,熔点为-40℃,沸点为71℃,不溶于冷水,易溶于有机溶剂,密度为1.65g/mL | Cl2与NH4Cl水溶液在低温下反应 | 95℃爆炸,热水中发生水解 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 25℃时,已知:
25℃时,已知:| A. | W 点所示的溶液中:c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(HCO3-) | |
| B. | pH=4 的溶液中:c(H2CO3)+c(HCO3-)+c(CO32-)=0.1 mol•L-1 | |
| C. | pH=8 的溶液中:c(H+)+c(H2CO3)+c(HCO3-)=c(OH-)+c(Cl-) | |
| D. | pH=11 的溶液中:CO32-+H2O HCO3-+OH- K≈1.8×l0-4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18 g H216O和20gH218O含有的质子数均为10 NA | |
| B. | l Ll mol/L的KAl(SO4)2溶液中阳离子总数为2 NA | |
| C. | 0.2 mol的铁与足量的稀硝酸反应,生成氢气的分子数目为0.3 NA | |
| D. | 反应N2+3H2?2NH3达平衡时,每消耗3 molH2同时有2 NA个N-H断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 微粒组 | 加人试剂 | 发生反应的离子方程式 |
| A | Fe3+、I-、Cr- | NaOH溶液 | Fe3++30H-═Fe(0H)3↓ |
| B | K+、NH3•H20、CO32- | 通人少量CO2 | 20H-+C02═CO32-+H20 |
| C | H+,Fe2+、SO42- | Ba(NO3)2溶液 | SO42-+Ba2+═BaSO4↓ |
| D | Na+、Al3+、Cl- | 少量澄淸石灰水 | Al3++30H-═Al(OH)3↓ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
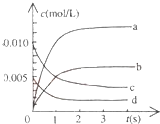 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.011 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com