
【题目】一定量的干燥甲烷燃烧后得到49.6g CO、CO2和H2O(g)组成的气体混合物,将此气体混合物全部缓缓通过足量的浓硫酸时气体质量减少25.2g,下列说法不正确的是( )
A. 产物中水的质量为25.2g B. 参加反应的甲烷为11.2g
C. 产物中CO的物质的量为0.4mol D. 产物中n(CO)=n(CO2)
【答案】D
【解析】A、无水氯化钙能够吸收水蒸气,气体质量减少25.2g,说明反应生成了25.2g水蒸气,故A正确;B、n(H2O)= ![]() =1.4mol,根据H原子守恒可计算CH4的物质的量为n(CH4)=
=1.4mol,根据H原子守恒可计算CH4的物质的量为n(CH4)= ![]() n(H2O)=
n(H2O)= ![]() ×1.4mol=0.7mol,甲烷的质量为0.7mol×16g/mol=11.2g,故B正确;C.根据C原子守恒,可知CO和CO2的总的物质的量为0.7mol,由于水的质量为25.2g,所以一氧化碳和二氧化碳的质量为49.6g-25.2g=24.4g,令CO、CO2的物质的量分别为xmol、ymol,则:x+y=0.7,28x+44y=22.4,解得x=0.4,y=0.3,故C正确;D.根据C的计算,CO、CO2的物质的量分别为0.4mol,0.3mol,故D错误;故选D。
×1.4mol=0.7mol,甲烷的质量为0.7mol×16g/mol=11.2g,故B正确;C.根据C原子守恒,可知CO和CO2的总的物质的量为0.7mol,由于水的质量为25.2g,所以一氧化碳和二氧化碳的质量为49.6g-25.2g=24.4g,令CO、CO2的物质的量分别为xmol、ymol,则:x+y=0.7,28x+44y=22.4,解得x=0.4,y=0.3,故C正确;D.根据C的计算,CO、CO2的物质的量分别为0.4mol,0.3mol,故D错误;故选D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】I.下列物质中,不属于芳香族化合物的是_______,属于芳香烃的是________,属于苯的同系物的是___________。(填编号)

II.己知某有机物的相对分子质量为58。根据下列条件回答:
若该有机物的组成只有C、H,则此有机物的分子式为______________;若它的核磁共振氢谱只有2个峰,则它的结构简式为______________,__________________。
III.有两个或两个以上的苯环以共有环边的方式相互稠合的多环芳香烃称为稠环芳香烃。下 图中椭圆烯也属于稠环芳香烃。据此回答:

(1)己知椭圆烯(I)的分子式为C24H12,则椭圆烯(II)的分子式为_______________;
(2)上述椭圆烯的一氯取代物各有几种同分异构体:(I)有_______种,(II)有_______种;
(3)假设上述椭圆烯可以和氢气在一定条件下发生加成反应生成饱和脂环烃,则加氢后的
生成物分子中所有的碳原子是否在同一平面内:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K2Cr2O7溶液中存在平衡:Cr2O72-(橙色)+H2O![]() 2CrO42-(黄色)+2H+。用K2Cr2O7溶液进行下列实验:
2CrO42-(黄色)+2H+。用K2Cr2O7溶液进行下列实验:
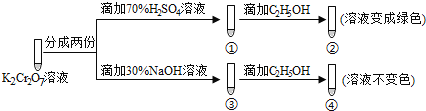
结合实验,下列说法不正确的是
A.①中溶液橙色加深,③中溶液变黄
B.②中Cr2O72-被C2H5OH还原
C.对比②和④可知K2Cr2O7酸性溶液氧化性强
D.若向④中加入70%H2SO4溶液至过量,溶液变为橙色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,某恒容密闭容器内有可逆反应:A(g)+3B(g)![]() 2C(g),该反应进行到一定限度后达到化学平衡的标志是( )
2C(g),该反应进行到一定限度后达到化学平衡的标志是( )
A. 3v正(A)=v逆(B)
B. 容器内气体的质量不随时间而改变
C. 容器内A、B、C三种物质的浓度相等
D. 容器内A、B、C的物质的量之比为1∶3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是氮元素在煤粉使用过程中的转化关系:

(1)③中加入的物质可以是___________(填标号)。
a.空气b.CO c.KNO3d.NH3
已知:N2(g) +O2(g)=2NO(g) △H = a kJ·mol-1
N2(g)+3H2(g)=2NH3(g) △H = b kJ·mol-1
2H2(g)+O2(g)=2H2O(l) △H = c kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H = d kJ·mol-1
上面转化关系反应后恢复至常温常压,根据以上信息写出③中你所选物质参与反应的热化学方程
式___________(如果所选物质不只一种,则只要写出其中一个热化学方程式即可)。
(2)将烟气中的氮氧化物(NOx)转化为无害物质,这个过程称为脱硝。下面反应为处理方法之一:
4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g)△H = -1625.5kJ·mol-1
4N2(g)+6H2O(g)△H = -1625.5kJ·mol-1
①若反应生成1molN2,则反应中转移的电子数为___________mol。
②使上述反应速率增大且平衡向右移动的措施是___________。
③氨氮比[n(NH3)/n(NO)]会直接影响该方法的脱硝率。350℃时,只改变氨气的投放量,反应物X的转化率与氨氮比的关系如图所示,则X是___________(填化学式)。在体积为2L的容器中模拟进行上述反应,初始时加入8molNO和3.5molO2,氨氮比为0.5时,该反应的平衡常数K =___________(保留二位小数)。当n(NH3)/n(NO)>1.0 时,烟气中NO浓度反而增大,主要原因是___________(用化学方程式表示)。

④若上述反应在与外界绝热的容器中进行,氨氮比由0.5增加到1.0时,在此过程中该反应的平衡常数___________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H2C2O4·xH2O)进行的探究性学习的过程,请你参与并协助他们完成相关学习任务。
该组同学的研究课题是:探究测定草酸晶体(H2C2O4·xH2O)中的x值。通过查阅资料和网络查寻得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:
2MnO![]() +5H2C2O4+6H+===2Mn2++10CO2↑+8H2O
+5H2C2O4+6H+===2Mn2++10CO2↑+8H2O
学习小组的同学设计了如下步骤用滴定的方法测定x值。
①称取1.260 g纯草酸晶体,将其制成100.00 mL水溶液为待测液。
②取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4。
③用浓度为0.1000 mol·L-1的酸性KMnO4标准溶液进行滴定,达到终点时消耗10.00 mL。
(1)上述步骤②中使用的锥形瓶是否需要事先用待测液润洗_______。(填“是”或“否”)滴定时,将酸性KMnO4标准液装在如图中的________(填“甲”或“乙”)滴定管中。

(2)本实验滴定达到终点的标志可以是________________________________。
(3)通过上述数据,求得x=________。
讨论:①若滴定终点时俯视滴定管刻度,则由此测得的x值会________(填“偏大”、“偏小”或“不变”,下同)。
②根据上述实验计算的数据可信性不强,为了提高实验的准确性,请写出改进方法______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求完成下列各小题实验.(a、b为弹簧夹,加热及固定装置已略去)

(1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸>碳酸)
① 实验步骤:连接仪器、 、加药品后,打开a关闭b,然后滴入浓硫酸,加热;
② 铜与浓硫酸反应的化学方程式 ,装置A中的试剂是 ;
③ 能说明碳的非金属性比硅强的实验现象是 ;
(2)验证SO2的氧化性、还原性和酸性氧化物的通性。
① 在(1)②操作后打开b,关闭a ;
② H2S溶液中有浅黄色浑浊出现,化学方程式是 ;
③ BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表中相应位置。

写出其中SO2显示还原性生成沉淀的离子方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com