
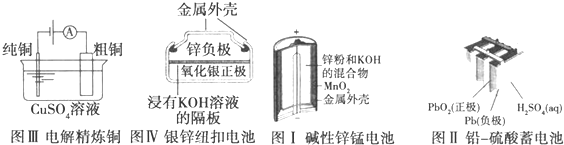
| A、图Ⅰ所示电池中,MnO2作催化剂 |
| B、图Ⅱ所示电池放电过程中,硫酸浓度不断增大 |
| C、图Ⅲ所示装置工作过程中,电解质溶液中Cu2+浓度始终不变 |
| D、图Ⅳ所示电池中,Ag2O作氧化剂,在电池工作过程中被还原为Ag |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| 取代苯甲醛 | 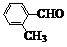 | 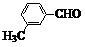 | 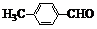 | 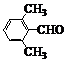 |
| 产率(%) | 15 | 23 | 33 | 0 |
| 取代苯甲醛 | 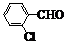 | 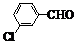 | 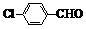 | 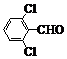 |
| 产率(%) | 71 | 63 | 52 | 82 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向加有酚酞的NaOH溶液中通入氯气,溶液立即褪色 |
| B、向加有酚酞的水中投入少量Na2O2粉末,溶液先变红,后褪色 |
| C、显红色的酚酞溶液中通入SO2后,红色褪去 |
| D、向溶有KMnO4的酸性溶液中通入SO2后,溶液紫红色褪去 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、低温下自发进行,高温下非自发进行 |
| B、任何温度下均为自发进行 |
| C、任何温度下均为非自发进行 |
| D、高温下自发进行,低温下非自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:
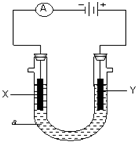 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.
电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4L氯仿(三氯甲烷)中共价键数目为4NA |
| B、标准状况下22.4升CH4和C2H4的混合气体所含氢原子数为4NA |
| C、25℃时,1L pH=1的稀H2SO4中有0.2 NA个H+ |
| D、理论上氢氧燃料电池正极消耗11.2 L标准状况下气体时,外电路通过电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,16g甲烷分子所含质子数为10NA |
| B、1 mol Cl2参加反应转移电子数一定为2NA |
| C、标准状况下,22.4L乙醇的分子数为NA |
| D、1 L 0.01 mol的Na2CO3溶液中含有0.01NA个CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com