
| A、7.8gNa2O2中所含阴离子的物质的量是0.2mol |
| B、等物质的量的-CH3与OH-所含电子数相等 |
| C、35Cl2和37Cl2互为同素异形体 |
| D、28.6gNa2CO3?10H2O晶体中含有CO32-数为0.1NA |


科目:高中化学 来源: 题型:
| A、大理石与盐酸反应放出CO2气体:CO32-+2H+=CO2+H2O |
| B、氧化钠与盐酸:O2-+2H+=H2O |
| C、碳酸氢钠与稀硫酸:CO32-+2H+=H2O+CO2↑ |
| D、醋酸与烧碱溶液混合:CH3COOH+OH-=CH3COO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 光照/叶绿素 |
| 催化剂 |
| △ |
| 催化剂 |
| △ |
| 催化剂 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
装置 | 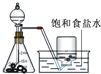 |  | 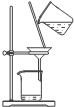 | 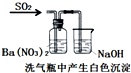 |
| 结论 | 用浓盐酸与二氧化锰制氯气 | 能证明非金属性 Cl>C>Si | 分离出Cl2与KI溶液反应生成的碘 | 白色沉淀一定是BaSO4 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、①④ | C、②③ | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、有大量的氯气泄漏时,用肥皂水浸湿软布蒙面,并迅速离开现场 |
| B、金属钠着火时,立即用水灭火 |
| C、蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 |
| D、用托盘天平称取5.85 g NaCl固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酸性高锰酸钾紫色溶液中加入植物油充分振荡后,溶液颜色不会褪去 |
| B、“地沟油”经过加工处理后,可以用来制造生物柴油 |
| C、铁粉、生石灰、硅胶是食品包装中常用的干燥剂 |
| D、鸡蛋清溶液中加入饱和硫酸钠溶液,生成的沉淀物不能再溶解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com