
 A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子.回答下列问题:
A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子.回答下列问题:分析 A、B、C、D为原子序数依次增大的四种元素,C、D为同周期元素,C核外电子总数是最外层电子数的3倍,则C为P元素;D元素最外层有一个未成对电子,D为Cl元素;
A2-和B+具有相同的电子构型,则A为O元素、B为Na元素;
(1)四种元素电负性最大的为O元素,C为P元素;
(2)A为O元素,有O2、O3两种同素异形体,O3相对分子质量较大,沸点较高,B的氢化物为NaH,为离子晶体;
(3)C和D反应可生成化合物为PCl3,为sp3杂化;
(4)化合物D2A为Cl2O,立体构型为V形,氯气与湿润的Na2CO3反应的方程式为2Cl2+2Na2CO3+H2O=Cl2O+2NaHCO3+2NaCl;
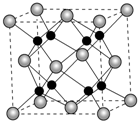
(5)A和B能够形成化合物F为离子化合物,阴离子位于晶胞的定点和面心,阳离子位于晶胞的体心,则Na的个数为8,O的个数为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,
N(Na):N(O)=2:1,则形成的化合物为Na2O,计算质量和体积,可计算密度.
解答 解:A、B、C、D为原子序数依次增大的四种元素,C、D为同周期元素,C核外电子总数是最外层电子数的3倍,则C为P元素;D元素最外层有一个未成对电子,D为Cl元素;
A2-和B+具有相同的电子构型,则A为O元素、B为Na元素;
(1)四种元素分别为O、Na、O、Cl,电负性最大的为O元素,C为P元素,核外电子排布为1s22s22p63s23p3,
故答案为:O;1s22s22p63s23p3;
(2)A为O元素,有O2、O3两种同素异形体,二者对应的晶体都为分子晶体,因O3相对分子质量较大,则范德华力较大,沸点较高,A的氢化物为水,为分子晶体,B的氢化物为NaH,为离子晶体,
故答案为:O3;O3相对分子质量较大,范德华力较大;分子晶体;离子晶体;
(3)C和D反应可生成组成比为1:3的化合物为PCl3,P形成3个δ键,孤电子对数为$\frac{5-3×1}{2}$=1,则为sp3杂化,立体构型为为三角锥形,
故答案为:三角锥形;sp3;
(4)化合物D2A为Cl2O,O为中心原子,形成2个δ键,孤电子对数为$\frac{6-2×1}{2}$=2,则中心原子的价层电子对数为4,立体构型为V形,
氯气与湿润的Na2CO3反应可制备Cl2O,反应的方程式为2Cl2+2Na2CO3+H2O=Cl2O+2NaHCO3+2NaCl,
故答案为:V形;4;2Cl2+2Na2CO3+H2O=Cl2O+2NaHCO3+2NaCl;
(5)A和B能够形成化合物F为离子化合物,阴离子位于晶胞的顶点和面心,阳离子位于晶胞的体心,则Na的个数为8,O的个数为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,
N(Na):N(O)=2:1,则形成的化合物为Na2O,
晶胞中O位于顶点,Na位于体心,每个晶胞中有1个Na与O的距离最近,每个定点为8个晶胞共有,则晶胞中O原子的配位数为8,
晶胞的质量为$\frac{4×62}{6.02×1{0}^{23}}$g,
晶胞的体积为(0.566×10-7)3cm3,
则晶体F的密度为$\frac{4×62}{(0.566×1{0}^{-7})^{3}×6.02×1{0}^{23}}$g•cm-3=2.27 g•cm-3,
故答案为:Na2O;8;2.27g•cm-3.
点评 本题考查物质结构和性质,为高频考点,侧重考查学生空间想象能力、知识运用能力,涉及晶胞计算、原子结构等知识点,采用均摊法、价层电子对互斥理论等理论分析解答,难点是晶胞计算,题目难度中等.


科目:高中化学 来源: 题型:多选题

| A. | 钢钉表面有白色沉淀 | B. | 实验2中的高锰酸钾溶液先变色 | ||
| C. | 负极的电极反应为:Fe-3e-→Fe3+ | D. | 铁钉表面有红褐色物质生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+、Al3+、NH4+、SO42- | B. | Ag+、NO3-、Na+、Ba2+ | ||
| C. | Fe2+、NO3-、SO42-、Na+ | D. | K+、CO32-、SO42-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
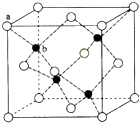 CuSO4在活化闪锌矿(主要成分是ZnS)方面有重要作用,主要是活化过程中生成CuS、Cu2S等一系列铜的硫化物活化组分.
CuSO4在活化闪锌矿(主要成分是ZnS)方面有重要作用,主要是活化过程中生成CuS、Cu2S等一系列铜的硫化物活化组分.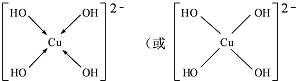 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
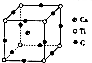 短周期元素A、B、C、D,A元素的原子最外层电子排布式为ms1,B元素的原子价电子排布式为ns2np2,C元素位于第二周期且原子中p能级与所有s能级电子总数相等,D元素原子的L层能级中有3个未成对电子.
短周期元素A、B、C、D,A元素的原子最外层电子排布式为ms1,B元素的原子价电子排布式为ns2np2,C元素位于第二周期且原子中p能级与所有s能级电子总数相等,D元素原子的L层能级中有3个未成对电子.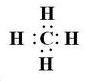 ,BC2属于非极性分子(填”极性“或”非极性“);当n=3时,B与C形成的晶体属于原子晶体.
,BC2属于非极性分子(填”极性“或”非极性“);当n=3时,B与C形成的晶体属于原子晶体.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑥ | B. | ②③④⑥ | C. | ③④⑤⑥ | D. | ⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
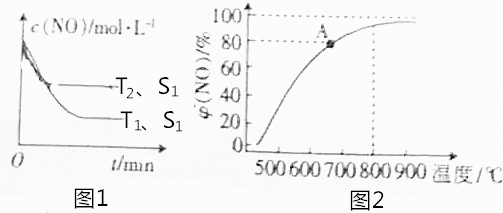
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
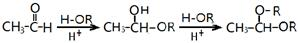

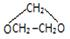 .
.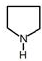 ,F
,F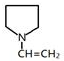 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com