
| A. | 温度升高不利于溴酸银的溶解 | |
| B. | 溴酸银的溶解是放热过程 | |
| C. | 若硝酸钾中含有少量溴酸银,可用重结晶方法提纯 | |
| D. | 60℃时,将0.04g溴酸银加入到10g水中,形成的分散系中存在沉淀溶解平衡 |
分析 A.温度升高溶解度增大;
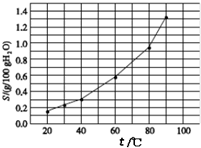
B.根据图象中温度对溴酸银的溶解度影响可知溴酸银的溶解过程为吸热过程;
C.溴酸银的溶解度受温度的影响较小,可以通过重结晶法分离硝酸钾与溴酸银的混合物;
D.根据溶解度计算10g水中溴酸银,结合选项中的数据判断是否饱和.
解答 解:A.温度升高溶解度增大,所以温度升高有于溴酸银的溶解,故A错误;
B.根据图象可知,升高温度,溴酸银的溶解度增大,说明溴酸银的溶解过程为吸热过程,故B错误;
C.根据图象可知,溴酸银的溶解度受温度的影响不大,而硝酸钾的溶解度受温度影响较大,所以硝酸钾中含有少量溴酸银,可用重结晶方法提纯,故C正确;
D.60℃时,溴酸银的溶解度为0.6g,则10g水中溴酸银的质量为0.06g,则0.04g溴酸银加入到10g水中形成不饱和溶液,则形成的分散系中不存在沉淀溶解平衡,
故D错误;
故选C.
点评 本题考查了难溶物的溶解平衡、温度对溶解度的影响等,题目难度中等,注意掌握难溶物的溶解平衡及其影响因素,明确溶度积的概念及计算方法是解题的关键.


科目:高中化学 来源: 题型:解答题
 2015年诺贝尔奖获得者屠呦呦提取的抗疟新药青蒿素的结构简式,用键线式表示如图.
2015年诺贝尔奖获得者屠呦呦提取的抗疟新药青蒿素的结构简式,用键线式表示如图. ,需要在有机合成中引入羟基,引入羟基的反应类型有①②⑤.(选填编号)
,需要在有机合成中引入羟基,引入羟基的反应类型有①②⑤.(选填编号)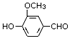 )可用于合成青蒿素,合成天然香草醛的反应如下:
)可用于合成青蒿素,合成天然香草醛的反应如下:
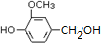 .
.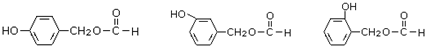 (其中之一).
(其中之一). 是合成青蒿素的中间原料之一,写出由苯甲醛和氯乙烷为原料,制备苄基乙醛的合成路线流程图(无机试剂任用).已知:羰基α-H可发生反应:
是合成青蒿素的中间原料之一,写出由苯甲醛和氯乙烷为原料,制备苄基乙醛的合成路线流程图(无机试剂任用).已知:羰基α-H可发生反应:
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 二氧化氯消毒液1000mL | |
| 溶质的质量分数 | 80% |
| 密度 | 1.2g/cm3 |
| 强腐蚀性,阴冷,密封储存 | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
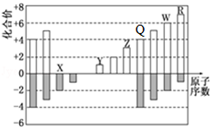
| A. | 原子半径:Z>Y>X | |
| B. | X和Z形成的化合物能溶于NaOH溶液 | |
| C. | Q和X形成的化合物不能与酸反应 | |
| D. | R元素的含氧酸和W元素的含氧酸,酸性一定前者强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | V1=V2=V3 | B. | V1>V3>V2 | C. | V2>V3>V1 | D. | V1>V2>V3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 温度 | pH=7 | pH=6 | pH=5 | pH=3 |
| 20℃ | 300 | 240 | 160 | 58 |
| 30℃ | 160 | 108 | 40 | 20 |
| 50℃ | 80 | 50 | x | 8 |
| A. | x可能为42 | |
| B. | 其他条件不变,在30°、pH=4下的反应速度比40℃、pH=6时快 | |
| C. | 根据单一变量法,无法比较温度、pH均不同的两组实验的反应速率较慢 | |
| D. | 30℃,pH=3条件下,KI的反应速率为v(KI)=0.005mol•L-1•s-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com