
| A. | 二者等物质的量完全燃烧消耗等量的氧气 | |
| B. | 二者分子所有原子都处于同一个平面上 | |
| C. | 二者能相互转化且反应属于可逆反应 | |
| D. | 二者可用酸性高锰酸钾溶液鉴别 |
分析 A.乙醇可将分子式拆写呈C2H4•H2O;
B.乙醇含有甲基,具有甲烷的结构特点;
C.二者能相互转化,但反应条件不同;
D.二者都可被酸性高锰酸钾氧化.
解答 解:A.乙烯分子式为C2H4,乙醇可将分子式拆写呈C2H4•H2O,二者等物质的量完全燃烧消耗等量的氧气,故A正确;
B.乙醇含有甲基,具有甲烷的结构特点,所有原子不可能处于同一个平面上,故B错误;
C.二者能相互转化,但反应条件不同,不是可逆反应,故C错误;
D.二者都可被酸性高锰酸钾氧化,不能用高锰酸钾鉴别,故D错误.
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物的组成、官能团与性质、有机反应等为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无法确定Al65Cu23Fe12中三种金属的化合价 | |
| B. | Al65Cu23Fe12的硬度小于金属铁 | |
| C. | Al65Cu23Fe12不可用作长期浸泡在海水中的材料 | |
| D. | 1mol Al65Cu23Fe12溶于过量的硝酸时共失去265 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 晶体硅是良好的半导体材料 | |
| B. | 硅单质可用来制造太阳能电池 | |
| C. | SiO2是制造光导纤维的材料 | |
| D. | 可用带玻璃塞的试剂瓶中盛有NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O | |
| B. | Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O | |
| C. | CH2=CH2+Br2→BrCH2-CH2Br | |
| D. | 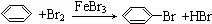 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
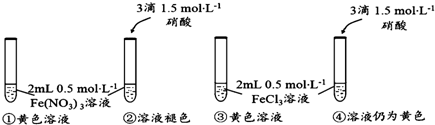

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Ca(HCO3)2溶液中加入足量的NaOH溶液:Ca2++HCO3-+OH-→CaCO3↓+H2O | |
| B. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2使SO42ˉ恰好完全反应:2Ba2++4OH-+Al3++2SO42-→BaSO4↓+AlO2-+2H2O | |
| C. | 足量的CO2通入饱和碳酸钠溶液中:CO2+CO32-+H2O→2HCO3- | |
| D. | 向Fe2(SO4)3溶液中加入过量Na2S溶液:2Fe3++3S2-→2FeS↓+S↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最高价氧化物水化物的碱性:Y<Z | B. | 简单气态氢化物的热稳定性:X<W | ||
| C. | X分别与Z、W形成化合物的熔点:Z<W | D. | 简单离子的还原性:X<W |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
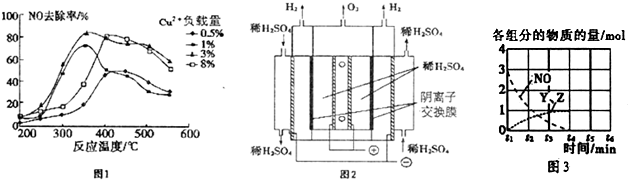
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com