
 根据如图中的两个图象,选出符合题意的反应方程式( )
根据如图中的两个图象,选出符合题意的反应方程式( )

科目:高中化学 来源: 题型:
(12分) X、Y、Z是阳离子,K是阴离子,M、N是中性分子。它们都由短周期组成,且具有以下结构特征和性质:
①它们核外电子总数都相同;
②N溶于M中,滴人酚酞,溶液变红;
③Y和K都由A、B两元素组成,Y核内质子总数比K多两个;
④X和N都由A、C两元素组成,X和Y核内质子总数相等;
⑤X和K的浓溶液在加热情况下生成M和N;
⑥Z为单核离子,向含有Z的溶液中加人少量K溶液,有白色沉淀生成,再加入过量的K或Y的溶液,沉淀消失。
试完成下列各题:
(1)Y的化学式为 ;X的电子式为 ;
(2)试比较M和N的稳定性:M N;
(3)写出Z和N的水溶液反应的离子方程式 ;
(4)上述六种微粒中的两种可与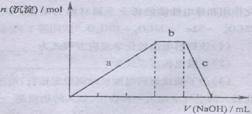 硫酸根形成一种复盐,向该盐的浓溶液中逐滴加入
硫酸根形成一种复盐,向该盐的浓溶液中逐滴加入![]() 的
的![]() 溶液,出现了如右图中a、b、c三个阶段的图象,根据图象判断该盐的化学式为 。
溶液,出现了如右图中a、b、c三个阶段的图象,根据图象判断该盐的化学式为 。
(5)将![]() g铜投入到一定量由A、B、C三种元素形成的一种常见化合物的溶液中,共收集到
g铜投入到一定量由A、B、C三种元素形成的一种常见化合物的溶液中,共收集到![]() 气体(标准状况下),将盛有此气体的容器倒扣在水槽中,通入一定量的氧气,恰好使气体完全溶于水,则通入氧气在标准状况下的体积是
气体(标准状况下),将盛有此气体的容器倒扣在水槽中,通入一定量的氧气,恰好使气体完全溶于水,则通入氧气在标准状况下的体积是 ![]() 。
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com