
| A. | 298K时,CaSO4的溶解度约为7.00×10-2mol/L | |
| B. | 反应CaSO4(s)+CO32-=CaCO3(s)+SO42-在298K时的平衡常数K=Ksp(CaSO4)/Ksp(CaCO3)=1.75×104 | |
| C. | CaCO3、CaSO4的饱和溶液的导电能力很弱,所以它们都是弱电解质 | |
| D. | 升高温度,两种盐的溶度积与溶解度都保持不变 |
分析 CaCO3、CaSO4都难溶于水,但为强电解质,可根据Ksp计算饱和溶液离子浓度,反应CaSO4(s)+CO32-=CaCO3(s)+SO42-的平衡常数K=$\frac{c(S{{O}_{4}}^{2-})}{c(C{{O}_{3}}^{2-})}$=$\frac{{K}_{sp}(CaS{O}_{4})}{{K}_{sp}(CaC{O}_{3})}$=$\frac{4.90×1{0}^{-5}}{2.80×1{0}^{-9}}$=1.75×104,以此解答该题.
解答 解:A.298K时,CaSO4的Ksp(CaCO3)=2.80×10-9,则c(CaCO3)=c(Ca2+)=$\sqrt{2.80×1{0}^{-9}}$mol/L=5.30×10-5mol/L,故A错误;
B.反应CaSO4(s)+CO32-=CaCO3(s)+SO42-的平衡常数K=$\frac{c(S{{O}_{4}}^{2-})}{c(C{{O}_{3}}^{2-})}$=$\frac{{K}_{sp}(CaS{O}_{4})}{{K}_{sp}(CaC{O}_{3})}$=$\frac{4.90×1{0}^{-5}}{2.80×1{0}^{-9}}$=1.75×104,故B正确;
C.CaCO3、CaSO4都难溶于水,但为强电解质,故C错误;
D.Ksp为温度的函数,升高温度,Ksp一定发生变化,故D错误.
故选B.
点评 本题侧重考查难溶物的溶解平衡,明确难溶物溶解平衡移动原理是解本题关键,为高频考点,注意把握溶度积的意义以及相关计算,难度不大.


 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:选择题
| A. | 在动力、设备、材料允许的条件下尽可能在高压下进行 | |
| B. | 温度越高越有利于工业合成氨 | |
| C. | 在工业合成氨中N2、H2的循环利用可提高其利用率,降低成本 | |
| D. | 及时从反应体系中分离出氨气有利于平衡向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu(OH) 2 | B. | Cu | C. | CuSO4 | D. | CuO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯甲酸的重结晶实验中要得到纯净的苯甲酸固体需要进行两次过滤操作 | |
| B. | 实验室制乙烯时,为减弱浓硫酸对有机物的碳化作用,应用小火缓慢加热 | |
| C. | 在石油的分馏、制硝基苯、制乙烯的实验中,都要使温度计的水银液泡浸入反应液中,以控制实验温度 | |
| D. | 制备硝基苯,混合药品的顺序为:向试管中先加入苯,再加入浓硫酸,最后加入浓硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
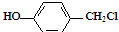 与NaOH水溶液共热,生成的有机物的结构简式为
与NaOH水溶液共热,生成的有机物的结构简式为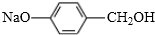 ;
; ;若该有机物有一个反式异构体,且能与氢气加成生成2-甲基戊烷,则该有机物的结构简式为
;若该有机物有一个反式异构体,且能与氢气加成生成2-甲基戊烷,则该有机物的结构简式为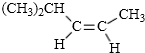 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca(HCO3)2 | B. | NaHCO3 | C. | Na2CO3 | D. | CaCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④③②① | B. | ①②③④ | C. | ③①②④ | D. | ③②①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com