
【题目】从元素组成上看,下列氧化物有一种明显与其他物质不同,它是
A. NO2 B. SO2 C. CaO D. CO2
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案科目:高中化学 来源: 题型:
【题目】丁烷在一定条件下裂解可按两种方式进行:C4H10 ![]() C2H6+C2H4 , C4H10
C2H6+C2H4 , C4H10 ![]() CH4+C3H6 .
CH4+C3H6 .
如图是某化学兴趣小组进行丁烷裂解的实验流程.(注:CuO能将烃氧化成CO2和H2O,G后面装置与答题无关,省略)
按上图连好装置后,需进行的实验操作有:①给D、G装置加热; ②检查整套装置的气密性; ③排出装置中的空气等…
(1)这三步操作的先后顺序依次是 .
(2)氧化铝的作用是 , 写出甲烷与氧化铜反应的化学方程式
(3)B装置所起的作用是 .
(4)若对E装置中的混合物(溴水足量),再按以下流程实验:
①操作I、操作II分别是、
②已知D的氢核磁共振谱图上只有一种峰,则D的结构简式
③Na2SO3溶液的作用是
(5)假定丁烷完全裂解,当(E+F)装置的总质量比反应前增加了0.7g,G装置的质量减少了1.76g,则丁烷的裂解产物中甲烷和乙烷的物质的量之比n (CH4):n (C2H6)=(假定流经D、G装置中的气体能完全反应)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气的化学性质很活泼,在一定条件下能与很多无机物和有机物反应,生成多种多样的含氯化合物。
(1)查阅文献:重铬酸钾与浓盐酸反应可以制备氯气。反应原理如下:K2Cr2O7+14HCl═2KCl+2CrCl3+3Cl2↑+7H2O
请在上述反应中标出电子转移的方向和数目。__________________
(2)图1是某同学制备氯水的装置图。

①装置B中发生反应的离子方程式为__________________。
②检验一瓶氯水是否已经完全变质,可选用的试剂是______________(填序号)。
A.硝酸银溶液B.酚酞溶液 C.碳酸钠溶液 D.紫色石蕊溶液
(3)漂白粉或漂白精的有效成分为Ca(ClO)2,Ca(ClO)2能与空气中的CO2和水蒸气发生如下反应:Ca(ClO)2+CO2+H2O = CaCO3↓+2HClO,分析以上反应,你认为存放漂白粉时应注意的问题有_________________________________________________。
(4)实验室欲用12 mol·L1的浓盐酸配制成250mL1.0 mol·L1的稀盐酸溶液。可供选择的仪器有:a.玻璃棒 b.烧瓶 c.烧杯 d.胶头滴管 e.量筒 f.托盘天平。
①上述仪器中,在配制稀盐酸溶液时不需要使用的有___________,还缺少的仪器是_____________。
②下列有关容量瓶的使用方法正确的是_____________(填代号)。
A.量筒量取浓盐酸试样后直接倒入容量瓶中,缓慢加水至接近刻度线1-2cm处,用胶头滴管加蒸馏水至刻度线
B.配制一定体积、浓度的溶液时,容量瓶未干燥,对所配溶液浓度无影响
C.容量瓶用水洗净后,再用1.0 mol·L1的稀盐酸溶液润洗
D.使用容量瓶前检查它是否漏水
③根据计算,本实验需要量取浓盐酸的体积为______mL(计算结果保留一位小数)。
④对所配制的稀盐酸进行测定,发现浓度大于1.0mol/L。请你分析配制过程中可能引起浓度偏高的原因(答出两点)___________________、________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于取代反应的是( )
A. 苯与液溴在铁粉存在下反应
B. 在镍做催化剂的条件下,苯与氢气反应
C. 乙烯的燃烧
D. 乙烯通入酸性高锰酸钾溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型纤维酸类降脂药克利贝特可由物质X在一定条件下反应制得,下列有关叙述正确的是( ) 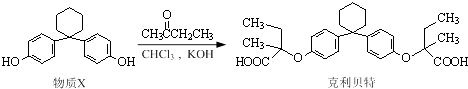
A.克利贝特的分子式为C28H34O6
B.物质X分子中所有碳原子可能位于同一平面内
C.用饱和NaHCO3溶液可以鉴别物质X和克利贝特
D.1 mol物质X最多可以与含2 molBr2的溴水反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上回收利用某合金废料(主要含Fe、Cu、Co、Li等,已知Co、Fe都是中等活泼金属)的工艺流程如下: 
(1)金属M为 , 操作1为 .
(2)加入H2O2的作用是(用离子方程式表示) , 加入氨水的作用是 .
(3)充分焙烧的化学方程式为 .
(4)已知Li2CO3微溶于水,其饱和溶液的浓度与温度关系见下表.操作2中,蒸发浓缩后必须趁热过滤,其原因是 , 90℃时Ksp(Li2CO3)的值为 .
温度/℃ | 10 | 30 | 60 | 90 |
浓度/molL﹣1 | 0.21 | 0.17 | 0.14 | 0.10 |
(5)用惰性电极电解熔融Li2CO3制取锂,阳极生成两种气体,则阳极的电极反应式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用括号内试剂除去下列各物质中的少量杂质,正确的是( )
A.溴苯中的溴(KI溶液)
B.乙烷中的乙烯(酸性高锰酸钾)
C.乙酸乙酯中的乙酸(饱和Na2CO3溶液)
D.苯中的甲苯(Br2水)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图转化关系中A﹣H为中学常见化合物,甲、乙、丙、丁为常见单质,其中甲、丁常温为气体,已知单质乙、化合物A为黄色(或淡黄色)固体,乙经过连续与甲反应后,再与水化合,是工业上制H的反应过程,B,F两种气体都能使澄清石灰水边浑浊(部分反应物或产物略去) 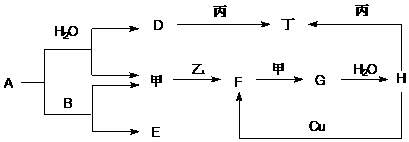
(1)写出物质A的电子式: .
(2)写出下列物质的化学式:甲乙丙 .
(3)写出A与H2O溶液反应的离子方程式 .
丙与D溶液反应的化学方程式 .
乙与D溶液反应的化学方程式 .
(4)常温下,H可用丙材料的容器盛装的原因是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com