
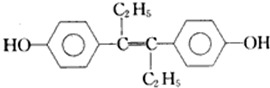
| A、该有机物分子中,最多可能有18个碳原子共平面 |
| B、该分子中有7个碳碳双键,可以与氢气1:7加成 |
| C、该分子对称性好,所以没有顺反异构 |
| D、标况下,1mol该有机物与足量金属钠反应可以放出22.4L的氢气 |


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
| A、一个分子中有12个五边形、20个六边形 |
| B、按凯库勒价键理论计算,12克足球烯可形成共价键的数目(共用电子对数)为1.5NA个 |
| C、按碳元素的四价理论计算,一个分子中有30个碳碳双键、60个碳碳单键 |
| D、N60分子与足球烯分子相似,每个氮原子的最外层电子数都满足8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①、② | B、①、③ |
| C、②、④ | D、②、③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
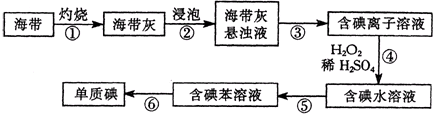
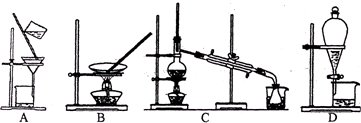
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示是某化学小组根据教材知识设计,说明Na2CO3与NaHCO3热稳定性的套管实验.下列叙述中不正确的是( )
如图所示是某化学小组根据教材知识设计,说明Na2CO3与NaHCO3热稳定性的套管实验.下列叙述中不正确的是( )| A、甲为NaHCO3,乙为Na2CO3 |
| B、要证明NaHCO3受热能产生水,可在小试管内放置沾有少量无水硫酸铜粉末的棉花球 |
| C、加热不久就能看到A烧杯中的澄清石灰水变浑浊 |
| D、整个实验过程中A烧杯中的澄清石灰水无明显变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O2具有漂白性 |
| B、均与水反应生成NaOH,因而均是碱性氧化物 |
| C、Na2O中氧-2价,Na2O2中氧-1价 |
| D、均可与H2O、CO2反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、集气瓶、水槽、药匙、量筒、玻璃棒 |
| B、托盘天平、大试管、玻璃棒、胶头滴管 |
| C、烧杯、容量瓶、玻璃棒、量筒、胶头滴管 |
| D、烧瓶、量筒、胶头滴管、玻璃棒、烧杯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用物质A表示的反应速率为1.2 mol/(L?s) |
| B、2 s时物质A的转化率为30% |
| C、用物质B表示的反应速率为0.6 mol/(L?s) |
| D、2 s时物质B的浓度为0.6 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
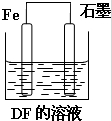 A、B、C、D、E、F六种短周期主族元素,其原子序数依次增大.A、D同主族;A与B、C均可形成多种常见的10电子微粒;在同一周期中,简单离子半径E的最小,原子半径F的最小;B的单质分子中有三对共用电子对.请回答下列问题:
A、B、C、D、E、F六种短周期主族元素,其原子序数依次增大.A、D同主族;A与B、C均可形成多种常见的10电子微粒;在同一周期中,简单离子半径E的最小,原子半径F的最小;B的单质分子中有三对共用电子对.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com