
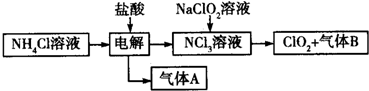
���� ���Ʊ����̿�֪����ⷢ��NH4Cl+2HCl$\frac{\underline{\;���\;}}{\;}$NCl3+3H2����Ȼ��NCl3��NaClO2ǡ�÷�Ӧ����ClO2���������Ȼ��ơ�NaOH����ϵ����غ��֪��ClԪ�صĻ��ϼ����ߣ���NԪ�ػ��ϼ۽��ͣ������ɰ�������÷�Ӧ�����ӷ�ӦΪNCl3+3H2O+6ClO2-=6ClO2��+3Cl-+3OH-+NH3�����Դ������
��� �⣺���Ʊ����̿�֪����ⷢ��NH4Cl+2HCl$\frac{\underline{\;���\;}}{\;}$NCl3+3H2����Ȼ��NCl3��NaClO2ǡ�÷�Ӧ����ClO2���������Ȼ��ơ�NaOH����ϵ����غ��֪��ClԪ�صĻ��ϼ����ߣ���NԪ�ػ��ϼ۽��ͣ������ɰ�������÷�Ӧ�����ӷ�ӦΪNCl3+3H2O+6ClO2-=6ClO2��+3Cl-+3OH-+NH3����
��1�����ʱ�������������ӵõ��������������������ĵ缫��ӦʽΪ2H++2e-=H2�������ʱ��Ӧ���ܷ���ʽΪNH4Cl+2HCl$\frac{\underline{\;���\;}}{\;}$NCl3+3H2�������NaClO3��Һ�ķ������ClO2������ClO2�ĵ缫��ӦʽΪClO3-+e-+H2O=ClO2��+2OH-��
�ʴ�Ϊ��NH4Cl+2HCl$\frac{\underline{\;���\;}}{\;}$NCl3+3H2����2H++2e-=H2����ClO3-+e-+H2O=ClO2��+2OH-��
��2��NCl3��NaClO2�����ʵ���֮��Ϊ1��6���ʱǡ�÷�Ӧ���ɵ��Ӻ�ԭ���غ��֪����ӦΪNCl3+3H2O+6NaClO2=6ClO2��+3NaCl+3NaOH+NH3����
�ʴ�Ϊ��NCl3+3H2O+6NaClO2=6ClO2��+3NaCl+3NaOH+NH3����
��3��ClO2������Ч�ʣ��Ե�λ���ʵ�����������ת�Ƶ�����Ŀ�Ķ���Ϊ���ݣ���Cl2��$\frac{1mol��[4-��-1��]}{1mol��2��[0-��-1��]}$=2.5�����ʴ�Ϊ��2.5��
���� ���⿼�����ʵ��Ʊ�ʵ�飬Ϊ��Ƶ���㣬�����Ʊ�ʵ�������з����ķ�ӦΪ���Ĺؼ������ط�����ʵ�顢�����������ۺϿ��飬��Ŀ�ѶȲ���


 �����ҵ���������ϵ�д�
�����ҵ���������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������õĵ����ԣ��������������� | |
| B�� | ͭ�Ļ�ѧ���ʲ����ã���˿������Ƶ��� | |
| C�� | �Ͼɵ���й��Ļ��տɼ��ٶԻ�������Ⱦ | |
| D�� | �ѺϽ��������кܺõġ������ԣ���˿�������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ȳʺ�ɫ����Һ�У�Fe2+��Cl-��NO3-��Na+ | |
| B�� | ʯ�����ɫ����Һ�У�K+��AlO2-��SiO32-��HSO3- | |
| C�� | ������Al3+����Һ�У�K+��Ca2+��NO3-��HCO3- | |
| D�� | ������OHһ����Һ�У�CO32-��ClO3-��F-��K+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
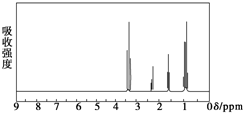 �˴Ź���������ָ�л�������е���ԭ�Ӻ������Ļ�ѧ���������丽���Ļ��ţ���ͬ�����ֳ��ĺ˴��ԾͲ�ͬ�������˴��������ķ��ں˴Ź���ͼ�������λ�ã���ѧλ�ƣ�����Ϊ�ģ�Ҳ�Ͳ�ͬ������һ���ʵĺ˴Ź���������ͼ��ʾ������������������еģ�������
�˴Ź���������ָ�л�������е���ԭ�Ӻ������Ļ�ѧ���������丽���Ļ��ţ���ͬ�����ֳ��ĺ˴��ԾͲ�ͬ�������˴��������ķ��ں˴Ź���ͼ�������λ�ã���ѧλ�ƣ�����Ϊ�ģ�Ҳ�Ͳ�ͬ������һ���ʵĺ˴Ź���������ͼ��ʾ������������������еģ�������| A�� | CH3CH2CH3 | B�� | CH3CH2CH2OH | C�� | 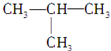 | D�� | CH3CH2CHO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 9�� | B�� | 10�� | C�� | 11�� | D�� | 12�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������Ư���ԣ��������ޡ��顢ֽ�ź�ʳƷ��Ư�� | |
| B�� | ���������ܽ���ˮ������������Һ��PM2.5�������ж����ЧӦ | |
| C�� | ��ˮ���ڻ�����Һ��������������ڴ����� | |
| D�� | SiO2���ܺ�NaOH��Һ��Ӧ���ܺ�����ᷴӦ������������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
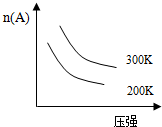
| A�� | 3A��g��+B��g��?2C��g������H��0 | B�� | A��g��+3B��s��+2C��g��?3D��g������H��0 | ||
| C�� | C��s��+D��g��?A��g��+B��g����H��0 | D�� | 2C��g��?2A��g��+B��g����H��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1 mol/L Na2CO3��Һ��c��OH-��=c��HCO3-��+c��H+��+c��H2CO3�� | |
| B�� | �����£�NH4Cl��NH3•H2O�����Һ��PH=7��c��NH4+ ��=c��Cl-�� | |
| C�� | �������Һ�м������������ƣ��õ��ļ��Ի����Һ��c��Na+����c��CH3COO-����c��H+����c��OH-�� | |
| D�� | �����£����������Һ�еμ�ϡ����õ���pH=5�Ļ����Һ��c��K+����c��NO3-�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com