
| A. | 反应液使酚酞试液变红色 | B. | 反应液使蓝色石蕊试纸变红色 | ||
| C. | 有大量固体析出 | D. | 反应后静置,反应液不分层 |
科目:高中化学 来源: 题型:选择题
| A. | NO2或N2O4的浓度不再变化 | B. | c(NO2)=c(N2O4) | ||
| C. | v正(NO2)=v逆(N2O4) | D. | NO2、N2O4的总质量不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜片电极反应:2H++2e-=H2↑ | B. | 锌片电极反应:Zn-e-=Zn2+ | ||
| C. | 铜为负极,发生还原反应 | D. | 锌为负极,发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧气 | B. | 硫磺 | C. | 木炭 | D. | 硝酸钾 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol烃基中电子数为10NA | |
| B. | 标准状况下,11.2L乙醇中含有的分子数为0.5NA | |
| C. | 标准状况下,0.56L丙烷中含有共价键的数目为0.2NA | |
| D. | 0.1mol乙烯和乙醇的混合物完全燃烧所消耗的氧原子数一定为0.6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
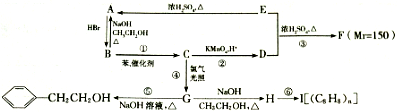
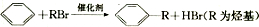 ;
; 可以在铁、稀盐酸作用下生成
可以在铁、稀盐酸作用下生成 ;
; .
. +CH3CH2OH$→_{△}^{浓硫酸}$
+CH3CH2OH$→_{△}^{浓硫酸}$ +H2O;
+H2O; ;
;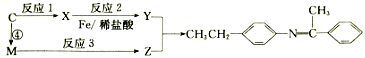
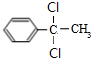 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com