
【题目】2008年北京奥运会的“祥云”火炬所用燃料的主要成分是丙烷,下列有关丙烷的叙述中不正确的是
A.分子中碳原子不在一条直线上B.比丁烷更易液化
C.1mol丙烷完全燃烧需消耗氧气5molD.光照下能够发生取代反应
科目:高中化学 来源: 题型:
【题目】向50 mL稀H2SO4与稀HNO3的混合溶液中逐渐加入铁粉,假设加入铁粉的质量与产生气体的体积(标准状况)之间的关系如下图所示,且每一段只对应一个反应。下列说法正确的

A. 开始时产生的气体为H2
B. AB段产生的反应为置换反应
C. 所用混合溶液中c(HNO3)=0.5mol·L-1
D. 参加反应铁粉的总质量m2=5.6 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NA为阿伏加德罗常数的数值,下列说法正确的是
A. 56g铁在足量氧气中燃烧,转移的电子数为2NA
B. lg氢气含有NA个氢气分子
C. 标准状况下,22.4L水含有1mol水分子
D. 2mol钠与过量稀盐酸反应生成NA个氢气分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中NO产生的反应为N2(g)+O2(g)![]() 2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,如图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述正确的是
2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,如图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述正确的是

A. 曲线b对应的条件改变可能是加入了催化剂
B. 温度T下,随着反应的进行,混合气体的密度减小
C. 温度T下,该反应的平衡常数K=![]()
D. 若曲线b对应的条件改变是温度,可判断该反应的ΔH<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化物是造成雾霾天气的主要原因之一,消除氮氧化物有多种方法。
(1)目前,应用最广泛的烟气氮氧化物脱除技术是NH3催化还原法,化学反应可表示为:
2NH3(g)+NO(g)+NO2(g)== 2N2(g)+3H2O(g) △H<0
①该反应中,反应物总能量_____(填“>”、“<”或“=”)生成物总能量。
②当该反应有2mol N2(g)生成时,转移电子的物质的量为__mol。
③该反应中,还原剂为______(填化学式),氧化产物与还原产物的质量比为______________。
(2)也可以利用甲烷催化还原氮氧化物.已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ/mol
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867kJ/mol
则CH4(g)将NO(g)还原为N2(g)的热化学方程式是_________________。
(3)还可利用ClO2消除氮氧化物的污染,反应过程如下(部分反应物或生成物略去):![]()
反应I的产物中还有两种强酸生成,且其中一种强酸为硝酸,且硝酸与NO3物质的量相等,则化学反应方程式为______,反应中若生成22.4L N2(标准状况),则消耗ClO2______g。
(4)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。

①氢氧燃料电池的能量转化主要形式是________,工作时电流方向为________(用a、b和箭头表示)。
②负极的电极反应式为__________________。
③电极表面镀铂粉的原因为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.100 0 mol/L NaOH溶液分别滴定20.00 mL 0.100 0 mol/L盐酸和20.00 mL 0.100 0 mol/L醋酸溶液,得到2条滴定曲线,如图所示。
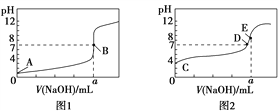
若以HA表示酸,下列说法不正确的是
A. 滴定盐酸的曲线是图1
B. 达到B、D状态时,两溶液中离子浓度均为c(Na+)=c(A-)
C. 达到B、E状态时,反应消耗的n(CH3COOH)=n(HCl)
D. 当0 mL<V(NaOH)<20.00 mL时,对应混合溶液中各离子浓度由大到小的顺序均为c(A-)>c(Na+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是
A.氯化铝溶液中加入过量氨水:Al3+ + 4NH3H2O =AlO2- + 4NH4+ + 2H2O
B.澄清石灰水与少量小苏打溶液混合:Ca2+ + OH- + HCO3- =CaCO3↓ + H2O
C.碳酸钙溶于醋酸:CaCO3 + 2H+=Ca2+ + CO2↑ + H2O
D.氯化铁溶液中加入单质铜:Fe3++Cu= Fe2+ + Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要配制0.50 mol/L NaCl溶液480 mL。按下列操作步骤填上适当的文字,以使整个操作完整。
(1)选择仪器。完成本实验所必需的仪器有:托盘天平(精确到0.1 g)、药匙、烧杯、玻璃棒、________、________以及等质量的两片滤纸。
(2)计算。配制该溶液需取NaCl晶体________g。
(3)称量。①天平调平之后,应将天平的游码调至某个位置
②称量过程中NaCl晶体应放于天平的________(填“左盘”或“右盘”)。
③称量完毕,将药品倒入烧杯中。
(4)溶解、冷却。该步实验中需要使用玻璃棒,目的是________________________。
(5)转移、洗涤。在转移时应使用________引流,需要洗涤烧杯2~3次是为了___________________。定容,摇匀。将配好的溶液静置一段时间后,倒入指定的试剂瓶,并贴好标签,注明配制的时间、溶液名称及浓度。
(6)在配制过程中,某学生观察定容时液面情况如图所示,所配溶液的浓度会__________(填“偏高”、“偏低”或“无影响”)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com