
 研究化学反应的快慢和限度具有十分重要的意义,请回答下列问题:
研究化学反应的快慢和限度具有十分重要的意义,请回答下列问题:分析 (1)升高温度,正逆反应的速率都增大;使用催化剂,正逆反应的速率都增大,但对平衡状态无影响;
(2)减缓反应速率,应降低浓度或降低反应温度,注意不影响生成氢气总量的要求;
(3)根据反应达平衡时,反应物生成物的量保持不变判断;根据物质的量的变化之比等于化学计量数之比书写方程式;
当反应达到平衡状态时,正、逆反应速率相等(同种物质),各物质的浓度、含量不再改变,以及由此衍生的一些物理量也不变,以此进行判断.
解答 解:(1)升高温度,正逆反应的速率都增大;使用催化剂,正逆反应的速率都增大,但对平衡状态无影响;故答案为:增大;增大;无;
(2)A.加入水,相当于将硫酸稀释,会减缓反应进行的速率,但是酸中氢离子的物质的量不变,所以不影响生成氢气的总量,故A正确;
B.加入KNO3固体,硝酸根与硫酸中的氢离子结合成硝酸,与锌反应不生成氢气,所以生成氢气的总量减小,故B错误;
C.加入硫酸钾溶液,溶液浓度减小,反应速率减小,但氢气的总量不受影响,故C正确;
D.加入KHSO4溶液,氢离子增多,生成氢气的总量增大,故D错误.
故选AC;
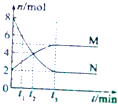
(3)随时间进行,t3时刻时M、N的物质的量不变且不为零,则反应为可逆反应并且达平衡,且△n(N):△n(M)=(8-2)mol:(5-2)mol=2:1,则反应的化学方程式为:2N?M;
A.由于随反应进行混合气体总物质的量发生变化,则压强一直在变,所以容器内的压强不再变化,能说明到达平衡,故A正确;
B.气体的颜色不再变化,说明有色气体N物质的量不变,能说明到达平衡,故B正确;
C.每反应2mol的N生成1mol的M,只指正反应方向,所以不能说明到达平衡,故C错误;
D.混合气体的总密度始终不随时间的变化而变化,不能说明到达平衡,故D错误;
故答案为:t3;2N?M;CD.
点评 本题考查化学反应速率的影响因素、化学平衡移动原理、化学平衡状态判断,难度不大,侧重对基础知识的巩固,注意判断化学平衡状态的物理量应随反应进行发生变化,该物理量由变化到不再变化说明到达平衡.


科目:高中化学 来源: 题型:选择题
| A. | 1:2 | B. | 2:1 | C. | 7:8 | D. | 8:7 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| a | 原子核外电子分别占3个不同能级,且每个能级上排布的电子数相同 |
| b | 基态原子的p轨道电子数比s轨道电子数少1 |
| c | 在周期表所列元素中电负性最大 |
| d | 基态原子M层全充满,N层只有一个电子 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X与W位于同一主族 | |
| B. | 原子半径:X>Y | |
| C. | 最简单氢化物的稳定性:X>Z | |
| D. | 最高价氧化物对应水化物的酸性:Z>W |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com