
【题目】己知:Mg(s)+2I H2O (g)=Mg(OH )2(s)+H2(g)△H1=﹣441kJmol﹣1
H2O(g)= ![]() H2(g)+O2(g)△H2=242kJmol﹣1
H2(g)+O2(g)△H2=242kJmol﹣1
Mg(s)+ ![]() O2(g)=MgO(s)△H3=﹣602kJmol﹣1
O2(g)=MgO(s)△H3=﹣602kJmol﹣1
①Mg(OH )2分解的热化学方程式为: .
②Mg(OH )2可以作为阻燃剂的原因(写一条即可) .
【答案】Mg(OH)2(s)=MgO(s)+H2O(g)△H=+81kJ?mol﹣1;Mg(OH )2分解要吸收大量的热,可以降低着火体系的温度
【解析】解:①Mg(s)+2H2O(g)=Mg(OH)2(s)+H2(g)△H1=﹣441kJmol﹣1 a,H2O(g)=H2(g)+ ![]() O2(g)△H2=+242kJmol﹣1 b,
O2(g)△H2=+242kJmol﹣1 b,
Mg(s)+ ![]() O2(g)=MgO(s)△H3=﹣602kJmol﹣1 c,
O2(g)=MgO(s)△H3=﹣602kJmol﹣1 c,
由盖斯定律可知b+c﹣a得到Mg(OH)2(s)=MgO(s)+H2O(g),则Mg(OH)2分解的热化学方程式Mg(OH)2(s)=MgO(s)+H2O(g)△H=+81kJmol﹣1 ;
所以答案是:Mg(OH)2(s)=MgO(s)+H2O(g)△H=+81kJmol﹣1 ;
②Mg(OH )2可以作为阻燃剂的原因为Mg(OH )2分解要吸收大量的热,可以降低着火体系的温度,
所以答案是:Mg(OH )2分解要吸收大量的热,可以降低着火体系的温度.


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】国家质检部门检出人们端午节包粽子的“返青粽叶”多以胆矾(化学式为CuSO4·5H2O)为添加剂,长期食用有害健康,请问胆矾是一种( )
A. 氧化物B. 盐C. 碱D. 酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某胶囊是一种常用的治疗胃酸过多的药品,其主要成分为一种两性氢氧化物。某同学欲对该胶囊内的白色固体的主要成分进行检验,设计了如下实验步骤:

(1) 操作Ⅱ所需要的玻璃仪器有_________、_________、________。
(2) 写出下列反应的方程式:
③的化学方程式:____________________________________________________,
④的离子方程式:______________________________________________________。
(3) 根据实验推测,该胃药的主要成分为_________________________________________。
(4) 该同学通过阅读课外读物了解到:常用胃药中除了上述实验已检出的物质外,还有NaHCO3,请你帮助该同学完成对滤液C中主要成分的探究实验(简要描述操作步骤):_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法,不正确的是
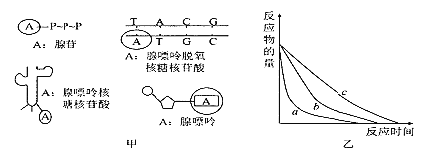
A. 甲图四种化合物中“0”内A所对应含义的解释有一个是错误的
B. 硝化细菌体内含有甲图中的四种化合物
C. 若乙图表示某种酶在不同温度下催化某反应的效果图,则温度a>b>c
D. 若乙图表示不同浓度的某种酶催化某反应的效果图,则酶浓度a>b>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热激活电池可用作火箭、导弹的工作电源.一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl﹣KCl混合物受热熔融后,电池即可瞬间输出电能.该电池总反应为PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.下列有关说法正确的是( ) 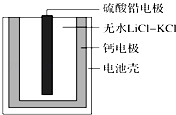
A.正极反应式:Ca+2Cl﹣﹣2e﹣=CaCl2
B.放电过程中,Li+向负极移动
C.常温时,在正负极间接上电流表或检流计,指针发生偏转
D.每转移0.1 mol电子,理论上生成10.35g Pb
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列三个化学反应的平衡常数(K1、K2、K3)与温度的关系分别如下表所示:请回答: 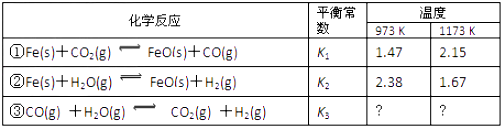
三个反应的平衡常数分别为K1、K2和K3推断反应③为△H30(填“>”成“<”)根据反应①和反应②可推导出K1、K2和K3的关系式:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的化合物在生产生活中广泛存在.
(1)处理生活污水中的NH4+ , 过程如图1: 
①根据较新的研究表明,将只含NO2﹣的污水与含NH4+的污水按比例混合,直接转化为无毒气体,该气体为 .
②空气将NH4+转变为NO3﹣或NO2﹣ , 溶液pH(填“增大”、“减小”或“不变”).
③完全处理含1mol NH4+污水,则n(O2)与n(CH3OH)关系式为[用n(O2)与n(CH3OH)表示].
(2)用焦炭还原NO2的反应为:2NO2(g)+2C(s )N2(g)+2CO2(g),在恒温条件下,1mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图2所示: 
①A、B两点的浓度平衡常数关系:Kc(A)Kc(B) (填“>”、“<”或“﹦”).
②A、B、C三点中NO2的转化率最高的是(填“A”或“B”或“C”)点.
③计算C点时该反应的压强平衡常数Kp(C)=(Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H7N9型禽流感是一种新型禽流感,研究表明,该病毒对热敏感,煮沸2分钟以上即可失去活性,许多常用消毒药物如:高锰酸钾、漂白粉、氯气等,也都可以将该病毒杀灭。
(1)新制氯水中含有多种微粒,将紫色石蕊试液滴入氯水中,溶液显红色起作用的微粒是____;过一会儿,溶液颜色逐渐褪去,起作用的微粒是______。
(2)工业上制取漂白粉的反应方程式为:___________。
(3)已知高锰酸钾与浓盐酸混合能产生氯气,化学反应方程式为:2KMnO4 +16HCl ![]() 2MnCl2+2KCl+8H2O+5Cl2↑
2MnCl2+2KCl+8H2O+5Cl2↑
该反应中氧化剂为________。请用双线桥法表示电子转移的情况。_________________
(4)向漂白粉清液中滴加碳酸钠溶液,有白色沉淀生成,写出发生反应的离子方程式___。
(5)将过量氯气通入FeBr2溶液中,写出该反应的离子方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将Na2O2逐渐加入到含有H+、Mg2+、Al3+、NH4+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入的Na2O2物质的量(mol)的关系如图所示,则原溶液中的Mg2+、Al3+、NH4+物质的量分别为

A. 2 mol、3 mol、6 mol B. 3 mol、2 mol、6mol
C. 2 mol、3 mol、4 mol D. 3 mol、2 mol、2 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com