


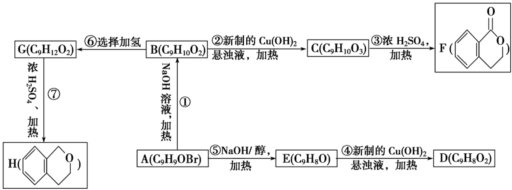
 ,H2MA发生缩聚反应得到PMLA为
,H2MA发生缩聚反应得到PMLA为 等,从G到H2MA发生水解、酸化,故G为
等,从G到H2MA发生水解、酸化,故G为 ,由D到G中官能团的变化可知,D为ClCH2CH=CHCH2Cl,D在氢氧化钠水溶液、加热条件下发生水解反应生成E为
,由D到G中官能团的变化可知,D为ClCH2CH=CHCH2Cl,D在氢氧化钠水溶液、加热条件下发生水解反应生成E为 ,E与HCl发生加成反应生成F为
,E与HCl发生加成反应生成F为 ,F与琼斯试剂反应得到G,据此解答.
,F与琼斯试剂反应得到G,据此解答. ,
, ;消去反应;
;消去反应; ,H2MA发生缩聚反应得到PMLA为
,H2MA发生缩聚反应得到PMLA为 等,从G到H2MA发生水解、酸化,故G为
等,从G到H2MA发生水解、酸化,故G为 ,由D到G中官能团的变化可知,D为ClCH2CH=CHCH2Cl,D在氢氧化钠水溶液、加热条件下发生水解反应生成E为
,由D到G中官能团的变化可知,D为ClCH2CH=CHCH2Cl,D在氢氧化钠水溶液、加热条件下发生水解反应生成E为 ,E与HCl发生加成反应生成F为
,E与HCl发生加成反应生成F为 ,F与琼斯试剂反应得到G,
,F与琼斯试剂反应得到G, ,故答案为:
,故答案为: ;
; ,故答案为:
,故答案为: ;
; ,
, ;
; 等,
等, 等.
等.


科目:高中化学 来源: 题型:
| 实验编号 | NaOH溶液的浓度 (mol/L) | 滴定完成时,消耗NaOH溶液的体积(mL) | 待测盐酸溶液的体积(mL) |
| 1 | 0.10 | 20.02 | 20.00 |
| 2 | 0.10 | 20.00 | 20.00 |
| 3 | 0.10 | 19.00 | 20.00 |
| 4 | 0.10 | 19.98 | 20.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有② | B、②④ |
| C、③④ | D、①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:

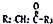
| NaOH(aq) |
| △ |
 +H2O(R1、R2、R3为烃基或氢原子)
+H2O(R1、R2、R3为烃基或氢原子) 中含有酚羟基所用的试剂是
中含有酚羟基所用的试剂是查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度(℃) | 0 | 10 | 30 | 50 | 56.7 | 60 | 64 | 70 | 80 | 90 | ||
| 溶解度(g/100g水) | 14.0 | 17.0 | 25.0 | 33.0 | 35.2 | 35.3 | 35.6 | 33.3 | 30.5 | 27.0 | ||
| 析出晶体 | FeSO4?7H2O | FeSO4?4H2O | FeSO4?H2O | |||||||||
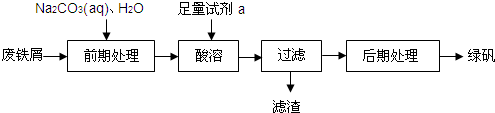


查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com