
【题目】(1)在______ molAl2(SO4)3中含0.3 mol SO42–,含Al3+约_______________个。
(2)同温同压下,相同质量的SO2气体和SO3气体,其分子数之比为_________,密度之比为_________。
(3)质量同为46 g的两种气体,NO2和N2O4,物质的量之比为________,二者所含O原子个数之比为_______。
【答案】0.11.204×10235︰44︰52︰11︰1
【解析】
(1)Al2(SO4)3中含0.3molSO42-,则n[Al2(SO4)3]=![]() n(SO42-)=
n(SO42-)=![]() ×0.3mol=0.1mol,n(Al3+)=2n[Al2(SO4)3]=0.1mol×2=0.2mol;即含Al3+约1.204×1023个;
×0.3mol=0.1mol,n(Al3+)=2n[Al2(SO4)3]=0.1mol×2=0.2mol;即含Al3+约1.204×1023个;
(2)相同质量的SO2气体和SO3气体,其分子数之比为![]() ×NA:
×NA:![]() ×NA=5:4;同温同压下,气体密度之比等于摩尔质量之比,故密度之比为64:80=4:5;
×NA=5:4;同温同压下,气体密度之比等于摩尔质量之比,故密度之比为64:80=4:5;
(3)NO2和N2O4的最简式相同,都为“NO2”,则等质量的NO2和N2O4,二者的物质的量之比为2:1,二者所含O原子个数之比为1:1。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】工业生产需要大量原料,消耗大量能源,在得到所需产品同时产生了大量废气、废水、废渣。某工厂排放的废水中含有Cu2+、Fe2+、Hg2+、H+等离子,某化学小组为了充分利用资源和保护环境,准备回收废水中的铜和汞,同时得到绿矾。他们设计了如下实验方案:
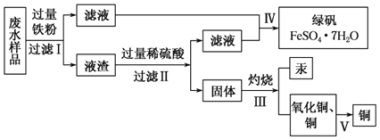
(1)步骤Ⅰ中加入过量铁粉的目的是_______________________________。
(2)步骤Ⅱ中________(填“能”或“不能”),用盐酸代替硫酸,写出步骤Ⅱ中涉及反应的化学方程式:____________________________________。
(3)步骤Ⅳ得到绿矾的操作蒸发浓缩______________、______________、洗涤、干燥。现有仪器:酒精灯、玻璃棒、坩埚、蒸发皿、蒸馏烧瓶、烧杯、铁架台等,完成步骤Ⅳ的实验操作还需要选择的玻璃仪器是___________。
(4)步骤 V利用氧化铜制取铜有如下四种方案:
方案甲:利用氢气还原氧化铜;方案乙:利用一氧化碳还原氧化铜;
方案丙:利用炭粉还原氧化铜;
方案丁:先将氧化铜溶于稀硫酸,然后加入过量的铁粉、过滤,再将滤渣溶于过量的稀硫酸,再过滤、洗涤、烘干。从安全角度考虑,方案_________不好;从产品纯度考虑,方案_________不好。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用石油产品A(C3H6)为主要原料,合成具有广泛用途的有机玻璃PMMA。流程如下(部分产物和条件省略)
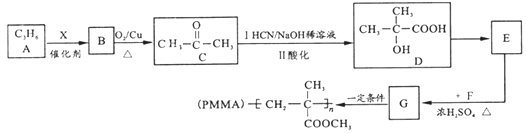
试回答下列问题:
(1)B的名称________;X试剂为_______(化学式);D中官能团名称_________。
(2)E→G的化学方程式为________________________________________,反应类型是_________。
(3)T是G的同分异构体,1molT与足量新制Cu(OH)2悬浊液反应最多生成2molCu2O沉淀,T的结构有________种(不含立体结构)。
(4)若高分子化合物PMMA的相对分子质量为1.5×106,其聚合度为_______。
(5)参照上述流程,以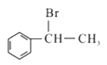 为原料合成
为原料合成 (其它原料自选)。设计合成路线:________________________。
(其它原料自选)。设计合成路线:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类比pH的定义,对于稀溶液可以定义pC=-lgC,pKa=-lgKa。常温下,某浓度H2A溶液在不同pH值下,测得pC(H2A)、pC(HA-)、pC(A2-)变化如图所示。下列说法正确的是
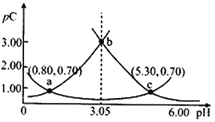
A. pH=3.50时,c(H2A)>c(HA-)>c(A2-)
B. 常温下,pKa1(H2A)=5.30,pKa2(H2A)=0.80
C. b点时,![]() =104.50
=104.50
D. pH=3.00~5.30时,c(H2A)+c(HA-)+c(A2-)先增大后减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下列实验装置完成相应的实验,能达到实验目的的是( )
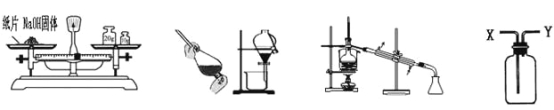
A. 称量NaOH固体 B. 用酒精提取溴水中的溴 C. 除去水中的氯化钠 D. 从Y进气收集CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下①6.72LCH4②3.01×1023个HCl分子③13.6gH2S④0.2molNH3,下列对这四种气体的关系从大到小表达正确的是( )
a.体积②>③>①>④ b.密度②>③>④>① c.质量②>③>①>④ d.氢原子个数①>③>④>②
A. abc B. bcd C. abcd D. acd
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,正确的是( )
A.硫酸的摩尔质量是98g
B.1mol N2的质量为28g/mol
C.摩尔是物质的量的单位
D.1mol氧的质量等于16g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种硫酸溶液,一种物质的量浓度为C1mol/L,密度为ρ1g/cm3,另一种物质的量浓度为C2mol/L,密度为ρ2g/cm3,当它们等体积混合后,溶液的密度为ρ3g/cm3,则混合溶液的物质的量浓度为
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com