
【题目】日常生活中遇到的很多问题都涉及化学知识,下列有关叙述不正确的是
A.Al2O3熔点高,可用作耐高温材料
B.用米汤检验含碘盐中的碘酸钾
C.用纯碱溶液洗涤餐具上的油污
D.利用丁达尔效应区别蛋白质溶液和食盐水
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)标准状况下11.2L NH3中含_________个氨分子, mol氢原子。
(2)等质量的SO2和SO3物质的量之比是 ;所含的氧原子个数之比是 。
(3)4.8gCH4中所含氢原子数与 g水所含氢原子数相等。
(4)含0.4mol A13+的Al2(SO4)3中所含的SO42﹣的物质的量是__________。
(5)已知16g A和20g B恰好完全反应生成0.04mol C和31.76g D,则C的摩尔质量为________。
(6)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物,则该化合物的化学式是__________。
(7)某盐混合溶液中含有离子:Na+、Mg2+、Cl﹣、SO42﹣,测得Na+、Mg2+ 和Cl﹣的物质的量浓度依次为:0.2molL﹣1、0.25molL﹣1、0.4molL﹣1,则c(SO42﹣)=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:① Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) ΔH=+489.0 kJ·mol-1
② CO(g)+![]() O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
③ C(石墨)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
则4Fe(s)+3O2(g)=2Fe2O3(s)的ΔH为( )
A.+1 164.1 kJ·mol-1 B.-1 641.0 kJ·mol-1
C.-259.7 kJ·mol-1 D.-519.4 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应叙述相符合的是( )

A. 图I:反应H2+I2![]() 2HI 达平衡后,升高温度时反应速率随时间的变化
2HI 达平衡后,升高温度时反应速率随时间的变化
B. 图Ⅱ:反应2SO2+O2![]() 2SO3达平衡后,缩小容器体积时各成分的物质的量随时间的变化
2SO3达平衡后,缩小容器体积时各成分的物质的量随时间的变化
C. 图III:反应N2+3H 2![]() 2NH3 在恒温情况下,反应速率与压强的关系
2NH3 在恒温情况下,反应速率与压强的关系
D. 图IV:反应CO2(g)+H2(g)![]() CO(g)+H2O(g)ΔH>0,水蒸气含量随时间的变化
CO(g)+H2O(g)ΔH>0,水蒸气含量随时间的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视____________。直到因加入一滴盐酸后,溶液由黄色变为橙色,并______________为止。
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是( )
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸 |
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥 |
C.酸式滴定管在滴定前有气泡,滴定后气泡消失 |
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数 |
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则终点读数为_____________mL。

(4)某学生根据3次实验分别记录有关数据如表:
滴定次数 | 待测NaOH溶液的体积/mL | 0.100 0 mol/L盐酸的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
第一次 | 25.00 | 0.10 | 26.11 | 26.01 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.32 | 26.31 | 25.99 |
依据上表数据列式计算该NaOH溶液的物质的量浓度为___________mol/L。(保留四位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中A到F是化合物,且A、B、E、F均含钠元素,G是单质。
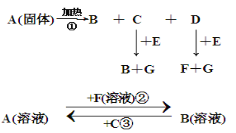
(1)写出A、B、E、F的化学式:A ,B ,E ,F 。
(2)写出反应①②③的化学方程式:
①
②
③
(3)写出D和E生成F和G的化学方程式,并用双线桥表示出电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 凡能发生银镜反应的有机物一定是醛
B. 在氧气中燃烧时只生成CO2和H2O的物质一定是烃
C. 苯酚有弱酸性,俗称石炭酸,因此它是一种羧酸
D. 在酯化反应中,羧酸脱去羧基中的羟基,醇脱去羟基中的氢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 氢氧化铝、碳酸钠都是常见的胃酸中和剂
B. 长期摄入肉、蛋、鱼偏多易导致血液偏酸性
C. 碘酒中的碘因有还原性而起到杀菌消毒作用
D. 碘盐、铁强化酱油等营养强化剂适合所有人食用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16,Ksp(Ag2CrO4)=2.0×10-12,则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是( )
A.AgCl>AgI>Ag2CrO4
B.AgCl>Ag2CrO4>AgI
C.Ag2CrO4>AgCl>AgI
D.Ag2CrO4>AgI>AgCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com