
| A£® | Ō×Ó°ė¾¶X£¼Y | B£® | ¾łÓŠ+3¼Ū | ||
| C£® | ×īĶā²ćµē×ÓŹż¾łĪŖ5 | D£® | ×īĶā²ć¾łÓŠ2øöµē×Ó |
·ÖĪö X”¢YĮ½ÖÖŌŖĖŲĪŖĶ¬Ņ»Ö÷×壬Ōņ×īĶā²ćµē×ÓŹżĻąµČ£¬ĒŅ¼Ū²ćµē×ÓŹżĻąµČ£¬ŅŌ“Ė½ā“šøĆĢā£®
½ā“š ½ā£ŗA£®Ō×Ó°ė¾¶“󊔲»ÄÜĖµĆ÷ŹĒ·ńĪŖĶ¬Ņ»Ö÷×壬¹ŹA“ķĪó£»
B£®N”¢Al¾łÓŠ+3¼Ū£¬µ«²»ŹĒĶ¬Ö÷×åŌŖĖŲ£¬¹ŹB“ķĪó£»
C£®×īĶā²ćµē×ÓŹż¾łĪŖ5£¬ĖµĆ÷¶¼ŹĒ¢õA×åŌŖĖŲ£¬¹ŹCÕżČ·£»
D£®Mg”¢He×īĶā²ć¾łÓŠ2øöµē×Ó£¬²»ŹĒĶ¬Ö÷×åÖ÷×åŌŖĖŲ£¬¹ŹD“ķĪó£®
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éŌŖĖŲÖÜĘŚ±ķµÄ½į¹¹¼°Ó¦ÓĆ£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕÖÜĘŚÖŠŌŖĖŲµÄÖÖĄąŹż¼°Ķ¬Ö÷×åŌ×ÓŠņŹżµÄ¹ŲĻµĪŖ½ā“šµÄ¹Ų¼ü£¬×¢ŅāŗĖĶāµē×ÓµÄÅŲ¼£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Cu”śCu2+ | B£® | SO32-”śSO2 | C£® | Fe2O3”śFe | D£® | MnO4-”śMn2+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1.8 gµÄNH4+Ąė×ÓÖŠŗ¬ÓŠµÄµē×ÓŹżĪŖ0.1NA | |
| B£® | 1mol Na2O2 ¹ĢĢåÖŠŗ¬Ąė×Ó×ÜŹżĪŖ4NA | |
| C£® | ±ź×¼×“æöĻĀ£¬2.24L CCl4Ėłŗ¬µÄ¹²¼Ū¼üŹżĪŖO.4NA | |
| D£® | ³£ĪĀ³£Ń¹ĻĀ£¬92g NO2ŗĶN2O4µÄ»ģŗĻĘųĢåŗ¬ÓŠµÄŌ×ÓŹżĪŖ6NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | K+”¢Ba2+”¢OH-”¢SO42- | B£® | Ag+”¢NO3-”¢Cl-”¢K+ | ||
| C£® | H3O+”¢NO3-”¢Fe2+”¢Na+ | D£® | Cu2+”¢NH4+”¢Br-”¢OH- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 365g 10%µÄŃĪĖį | B£® | 22.4L ĀČ»ÆĒā £ØŅŃÖŖĆܶČĪŖ1.7g/L£© | ||
| C£® | 36.5g HClĘųĢ壮 | D£® | 0.5mol HClĘųĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | RŹĒ·¼ĻćĢž | B£® | Rŗ¬2ÖÖŗ¬Ńõ¹ŁÄÜĶÅ | ||
| C£® | 1mol R×ī¶ąÓė1molH2¼Ó³É | D£® | RÄÜ·¢Éś¼Ó³É”¢Č”“śŗĶŃõ»Æ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | K+”¢Na+”¢HCO${\;}_{3}^{-}$”¢Cl- | B£® | Fe3+”¢SCN-”¢Cl-”¢SO${\;}_{4}^{2-}$ | ||
| C£® | NH${\;}_{4}^{+}$”¢Fe2+”¢SO${\;}_{4}^{2-}$”¢NO${\;}_{3}^{-}$ | D£® | Mg2+”¢Fe2+”¢SO${\;}_{4}^{2-}$”¢Cl- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
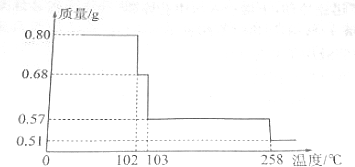
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com