
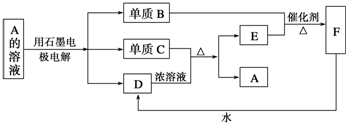
分析 电解A溶液得到三种物质,应是电解水及A,且有两种单质生成,则D为碱或酸,且单质C能与D浓溶液反应得到A,D不能为碱,只能为酸,可推知B为氧气、C为Cu、D为硫酸,E为二氧化硫,F为三氧化硫,A为硫酸铜,据此解答.
解答 解:电解A溶液得到三种物质,应是电解水及A,且有两种单质生成,则D为碱或酸,且单质C能与D浓溶液反应得到A,D不能为碱,只能为酸,可推知B为氧气、C为Cu、D为硫酸,E为二氧化硫,F为三氧化硫,A为硫酸铜,
(1)由上述分析可知,A为CuSO4,D为H2SO4,F为SO3,
故答案为:CuSO4;H2SO4;SO3;
(2)C和D的浓溶液反应化学方程式为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,
故答案为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
(3)电解硫酸铜溶液时反应的化学方程式为:2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2H2SO4+2Cu+O2↑,
故答案为:2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2H2SO4+2Cu+O2↑.
点评 本题考查无机物推断,涉及电解原理、硫元素化合物性质,难度中等,注意根据电解产物作为突破口推断.


科目:高中化学 来源:2016-2017学年山东省高二上10月月考化学卷(解析版) 题型:选择题
下列有关说法正确的是
A.反应2CO(g)=2C(s)+O2(g) △H>0可以自发进行
B.放热反应在常温条件下一定很容易进行
C.平衡常数发生变化,化学平衡一定发生移动
D.化学平衡发生移动,平衡常数一定发生改变
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高一上10月月考化学卷(解析版) 题型:选择题
在标准状况下,1体积水溶解700体积NH3,所得溶液密度为0.9g·cm-3,这种氨水的物质的量浓度和溶质的质量分数分别为
A.18.4mol·L-1、34.7% B.20.4mol·L-1、38.5%
C.18.4mol·L-1、38.5% D.20.4mol·L-1、34.7%
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +45.2 kJ•mol-1 | B. | -45.2 kJ•mol-1 | C. | -69.4 kJ•mol-1 | D. | +69.4 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO - | |
| B. | NaAlO2溶液中通入过量的CO2:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- | |
| C. | 用稀HNO3溶解Fe3O4固体的离子方程式:Fe3O4+8H+═2Fe3++Fe2++4H2O | |
| D. | NaHCO3溶液中加少量Ba(OH)2溶液:2HCO3-+Ba2++2OH-═BaCO3↓+2H2O+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 溶质的电离方程式为NaHCO3═Na++H++CO32- | |
| B. | 25℃时,加水稀释后,c(H+)与c(OH-)的乘积不变 | |
| C. | 离子浓度关系:c(Na+)+c(H+)═c(OH-)+c(HCO3-)+c(CO32-) | |
| D. | 温度升高,c(HCO3-)减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 阳极 | 石墨棒 | Cu | Cu | Cu |
| 阴极 | 石墨棒 | Fe | 石墨棒 | Pt |
| 电解液 | CuSO4溶液 | H2SO4溶液 | Na2SO4溶液 | H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com