
(14分)
Ⅰ、实验室常用以下方法制取氯气:MnO2+ 4HCl(浓) 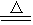 MnCl2+Cl2↑ + 2H2O,
MnCl2+Cl2↑ + 2H2O,
(1)用双线桥标出电子转移方向和数目。(在答题纸上标)
(2)在标准状况下生成的Cl2为11.2L时,参加反应的HCl的物质的量为 ,
被氧化HCl的质量为 。
Ⅱ、科学家发现,食用虾类等水生甲壳类动物的同时服用维生素C容易中毒。这是因为
对人体无害的+5价砷类化合物在维生素C的作用下,能够转化为有毒的+3价的含砷化
合物。通过以上信息填空:
(1)维生素C具有 (填氧化性或还原性)。
(2)上述过程中+5价砷类物质作为 (填氧化剂或还原剂),+5价砷元素发生
反应(填氧化或还原);2mol +5价砷完全转化为 +3价砷,共转移 个
电子(用NA表示阿伏加德罗常数)。
(每空2分,共14分)
Ⅰ、(1) (2)2mol,36.5g。
(2)2mol,36.5g。
Ⅱ、(1) 还原性 (2)氧化剂 ; 还原 ;4NA
解析试题分析:Ⅰ、(1)根据反应的方程式可知,盐酸中氯元素的化合价从-1价升高到0价,失去1个电子。而二氧化锰中Mn元素的化合价从+4价降低到+2价,得到2个电子,所以根据电子到得失守恒可知,正确的表示应该是 。
。
(2)氯气的物质的量是11.2L÷22.4L/mol=0.5mol,则根据反应的化学方程式可知,参加反应的氯化氢是0.5mol×4=2mol。其中被氧化的氯化氢是1mol,质量是36.5g。
Ⅱ、(1)+5价砷类化合物在维生素C的作用下,能够转化为有毒的+3价的含砷化,这说明砷元素得到电子,所以维生素C失去电子,具有还原性。
(2)As元素的化合价从+5价降低到+3价,得到2个电子,做氧化剂,则+5价砷元素发生还原反应。2mol +5价砷完全转化为 +3价砷,得到4mol电子,则共转移4NA个电子。
考点:考查氧化还原反应的表示、计算以及有关判断
点评:该题是基础性试题的考查,也是高考中的常见考点,难度不大。试题放热关键是熟练掌握氧化还原反应的有关概念,判断的依据,然后再结合题意灵活分析即可。该题有利于培养学生分析问题、解决问题的能力。


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.玻璃棒是中学化学实验室中常用的仪器。下列实验过程中,一般不需要用玻璃棒的是
(填写编号)
①用pH试纸测定Na2CO3溶液的pH ②配制一定物质的量浓度的氯化钠溶液 ③将适量氯化铁饱和溶液滴入沸水中制备氢氧化铁胶体 ④探究Ba(OH)2![]() 8H20晶体和NH4Cl晶体反应过程中的能量变化 ⑤用蒸馏法分离两种沸点差距较大的液体 ⑥过滤分离互不相溶的固体和液体 ⑦用已知浓度的盐酸滴定待测浓度的NaOH溶液的酸碱中和滴定过程 ⑧稀释浓H2SO4的过程
8H20晶体和NH4Cl晶体反应过程中的能量变化 ⑤用蒸馏法分离两种沸点差距较大的液体 ⑥过滤分离互不相溶的固体和液体 ⑦用已知浓度的盐酸滴定待测浓度的NaOH溶液的酸碱中和滴定过程 ⑧稀释浓H2SO4的过程
Ⅱ.为测定某含有杂质Na2O的Na2O2样品的纯度,某小组同学分别设计了如下方案。
【方案一】准确称量样品mg,与水充分反应后将溶液的体积稀释为VmL,从中取出V1mL溶液,装入锥形瓶,用已知浓度的盐酸进行滴定,以确定溶液的浓度,再计算出样品中Na2O2的含量。
⑴此方案中,酸碱中和滴定时应选用 滴定管。
⑵写出此方案中涉及到的反应的离子方程式 。
【方案二】准确称量样品mg,将样品与二氧化碳充分反应,通过测定反应产生氧气的体积,计算出样品中Na2O2的含量。
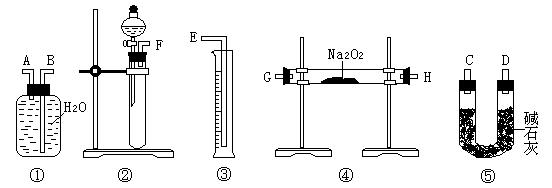
⑶该方案的实验过程中,仪器的连接顺序是 (填仪器下方序号),①中的进气口为 (填“A”或“B”)
⑷装置⑤的作用是 。
⑸你认为方案一、方案二中测定结果比较准确的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(14分)
Ⅰ.玻璃棒是中学化学实验室中常用的仪器。下列实验过程中,一般不需要用玻璃棒的是
(填写编号)
①用pH试纸测定Na2CO3溶液的pH ②配制一定物质的量浓度的氯化钠溶液③将适量氯化铁饱和溶液滴入沸水中制备氢氧化铁胶体④探究Ba(OH)2![]() 8H20晶体和NH4Cl晶体反应过程中的能量变化 ⑤用蒸馏法分离两种沸点差距较大的液体 ⑥过滤分离互不相溶的固体和液体⑦用已知浓度的盐酸滴定待测浓度的NaOH溶液的酸碱中和滴定过程 ⑧稀释浓H2SO4的过程
8H20晶体和NH4Cl晶体反应过程中的能量变化 ⑤用蒸馏法分离两种沸点差距较大的液体 ⑥过滤分离互不相溶的固体和液体⑦用已知浓度的盐酸滴定待测浓度的NaOH溶液的酸碱中和滴定过程 ⑧稀释浓H2SO4的过程
Ⅱ.为测定某含有杂质Na2O的Na2O2样品的纯度,某小组同学分别设计了如下方案。
【方案一】准确称量样品mg,与水充分反应后将溶液的体积稀释为VmL,从中取出V1mL溶液,装入锥形瓶,用已知浓度的盐酸进行滴定,以确定溶液的浓度,再计算出样品中Na2O2的含量。
⑴此方案中,酸碱中和滴定时应选用 滴定管。
⑵写出此方案中涉及到的反应的离子方程式 。
【方案二】准确称量样品mg,将样品与二氧化碳充分反应,通过测定反应产生氧气的体积,计算出样品中Na2O2的含量。
⑶该方案的实验过程中,仪器的连接顺序是 (填仪器下方序号),①中的进气口为 (填“A”或“B”)
⑷装置⑤的作用是 。
⑸你认为方案一、方案二中测定结果比较准确的是 。
查看答案和解析>>
科目:高中化学 来源:辽宁省抚顺市六校联合体2009—2010学年度高三二模(理综)试题化学部分 题型:实验题
(14分)
Ⅰ.玻璃棒是中学化学实验室中常用的仪器。下列实验过程中,一般不需要用玻璃棒的是
(填写编号)
①用pH试纸测定Na2CO3溶液的pH ②配制一定物质的量浓度的氯化钠溶液③将适量氯化铁饱和溶液滴入沸水中制备氢氧化铁胶体④探究Ba(OH)2 8H20晶体和NH4Cl晶体反应过程中的能量变化⑤用蒸馏法分离两种沸点差距较大的液体⑥过滤分离互不相溶的固体和液体⑦用已知浓度的盐酸滴定待测浓度的NaOH溶液的酸碱中和滴定过程⑧稀释浓H2SO4的过程
8H20晶体和NH4Cl晶体反应过程中的能量变化⑤用蒸馏法分离两种沸点差距较大的液体⑥过滤分离互不相溶的固体和液体⑦用已知浓度的盐酸滴定待测浓度的NaOH溶液的酸碱中和滴定过程⑧稀释浓H2SO4的过程
Ⅱ.为测定某含有杂质Na2O的Na2O2样品的纯度,某小组同学分别设计了如下方案。
【方案一】准确称量样品mg,与水充分反应后将溶液的体积稀释为VmL,从中取出V1mL溶液,装入锥形瓶,用已知浓度的盐酸进行滴定,以确定溶液的浓度,再计算出样品中Na2O2的含量。
⑴此方案中,酸碱中和滴定时应选用 滴定管。
⑵写出此方案中涉及到的反应的离子方程式 。
【方案二】准确称量样品mg,将样品与二氧化碳充分反应,通过测定反应产生氧气的体积,计算出样品中Na2O2的含量。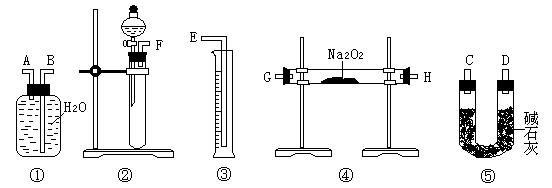
⑶该方案的实验过程中,仪器的连接顺序是 (填仪器下方序号),①中的进气口为 (填“A”或“B”)
⑷装置⑤的作用是 。
⑸你认为方案一、方案二中测定结果比较准确的是 。
查看答案和解析>>
科目:高中化学 来源:辽宁省抚顺市六校联合体2009-2010学年度高三二模(理综)试题化学部分 题型:实验题
(14分)
Ⅰ.玻璃棒是中学化学实验室中常用的仪器。下列实验过程中,一般不需要用玻璃棒的是
(填写编号)
①用pH试纸测定Na2CO3溶液的pH ②配制一定物质的量浓度的氯化钠溶液
③将适量氯化铁饱和溶液滴入沸水中制备氢氧化铁胶体
④探究Ba(OH)2 8H20晶体和NH4Cl晶体反应过程中的能量变化 ⑤用蒸馏法分离两种沸点差距较大的液体 ⑥过滤分离互不相溶的固体和液体
⑦用已知浓度的盐酸滴定待测浓度的NaOH溶液的酸碱中和滴定过程 ⑧稀释浓H2SO4的过程
8H20晶体和NH4Cl晶体反应过程中的能量变化 ⑤用蒸馏法分离两种沸点差距较大的液体 ⑥过滤分离互不相溶的固体和液体
⑦用已知浓度的盐酸滴定待测浓度的NaOH溶液的酸碱中和滴定过程 ⑧稀释浓H2SO4的过程
Ⅱ.为测定某含有杂质Na2O的Na2O2样品的纯度,某小组同学分别设计了如下方案。
【方案一】准确称量样品mg,与水充分反应后将溶液的体积稀释为VmL,从中取出V1mL溶液,装入锥形瓶,用已知浓度的盐酸进行滴定,以确定溶液的浓度,再计算出样品中Na2O2的含量。
⑴此方案中,酸碱中和滴定时应选用 滴定管。
⑵写出此方案中涉及到的反应的离子方程式 。
【方案二】准确称量样品mg,将样品与二氧化碳充分反应,通过测定反应产生氧气的体积,计算出样品中Na2O2的含量。
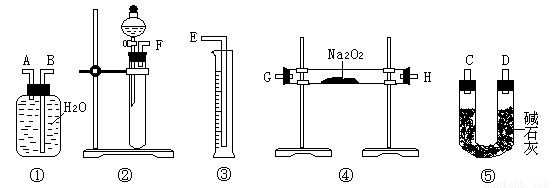
⑶该方案的实验过程中,仪器的连接顺序是 (填仪器下方序号),①中的进气口为 (填“A”或“B”)
⑷装置⑤的作用是 。
⑸你认为方案一、方案二中测定结果比较准确的是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com