
分析 根据农作物对两种化肥的吸收情况以及两种化肥的组成分析:植物吸收营养元素的原理是通过交换吸附来进行的,吸附之后不能改变土壤酸碱性的肥料适宜,两种肥料的区别是(NH4)2SO4只有阳离子含有植物营养元素N元素,而NH4NO3中阴阳离子都含有N元素,且施用(NH4)2SO4时,交换吸附后进入土壤的H+多,吸收SO42-少,土壤显酸性,据此分析.
解答 解:植物吸收营养元素的原理是通过交换吸附来进行的,(NH4)2SO4只有阳离子含有植物营养元素N元素,而NH4NO3中阴阳离子都含有N元素,施用(NH4)2SO4时,植物需氮多,吸收NH4+多,吸收SO42-少.交换吸附后进入土壤的H+多,使土壤显酸性,故不适于酸性土壤;若用NH4NO3,植物对NH4+和NO3-的吸收量相同,交换吸附后进入土壤的H+和OH-的量相同,不会增加土壤的酸性,故适于酸性土壤,
答:施用(NH4)2SO4时,吸收NH4+多,吸收SO42-少,容易使土壤的酸性更强,施用NH4NO3时,植物对NH4+和NO3-的吸收量相同,对土壤的影响比硫酸铵小.
点评 本题考查酸性土壤中氮肥的选择,掌握植物对土壤中营养元素吸收的原理,了解不同的肥料被吸收的方式的不同是解题的关键,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
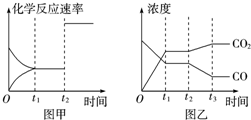
| 温度 | K1 | K2 |
| 973K | 1.47 | 2.38 |
| 1173K | 2.15 | 1.67 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 盐酸、硫酸和硝酸是中学阶段常见的“三大酸”.现就硫酸、硝酸与金属铜反应的情况,回答下列问题:
盐酸、硫酸和硝酸是中学阶段常见的“三大酸”.现就硫酸、硝酸与金属铜反应的情况,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 黄绿色的氯水光照后颜色变浅 | |
| B. | 在硫酸亚铁溶液中,加入铁粉以防止氧化变质 | |
| C. | 生产硝酸的过程中使用过量空气以提高氨气的利用率 | |
| D. | 实验室常用排饱和食盐水的方法收集氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二元弱酸酸式盐NaHA溶液中:c(H+)+c(Na+)=c(OH-)+c(HA-)+c(A2-) | |
| B. | 一定量的(NH4)2SO4与NH3•H2O混合的酸性溶液中:c(NH4+)>2c(SO42-) | |
| C. | 物质的量浓度均为0.01mol/L的CH3COOH和CH3COONa的溶液等体积混合后溶液中 c(CH3COOH)+c(CH3COO-)=0.02 mol/L | |
| D. | 物质的量浓度相等的①NH4HSO4溶液、②NH4HCO3溶液、③NH4Cl溶液中c(NH4+):①>③>② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
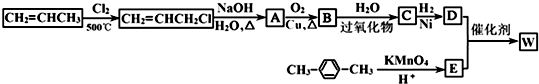
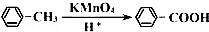
 .
.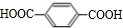 →
→ +2H2O.
+2H2O.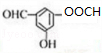 .
.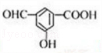 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ② | C. | ③④ | D. | ④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com