
【题目】丁苯酞是一种治疗急性脑缺血的药物,部分合成流程如下。下列说法正确的是( )
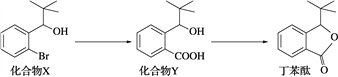
A. 化合物X、Y和丁苯酞三种分子中各含有1个手性碳原子
B. 化合物Y可以发生取代、加成和加聚反应
C. 可用Na2CO3溶液鉴别化合物X和化合物Y
D. 化合物X、Y和丁苯酞各1 mol最多消耗NaOH的量均为1 mol
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:
【题目】(1)已知:4NH3(g)+6NO(g)=5N2(g)+6H2O(l) ΔH1 4NH3(g)+5O2(g)=4NO(g)+6H2O(l) ΔH2
则 NH3(g)的标准燃烧热Δ H=__________________。
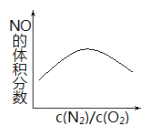
(2)高温下,N2(g)+O2(g)![]() 2NO(g), ΔH<0,反应达到平衡时混合气体中NO的体积分数与反应物中 c(N2)/c(O2)的比值的关系如图,请在右图上画出适当降温后,反应达到平衡时混合气体中 NO 的体积分数与反应物中 c(N2)/c(O2)的比值的关系图。_______
2NO(g), ΔH<0,反应达到平衡时混合气体中NO的体积分数与反应物中 c(N2)/c(O2)的比值的关系如图,请在右图上画出适当降温后,反应达到平衡时混合气体中 NO 的体积分数与反应物中 c(N2)/c(O2)的比值的关系图。_______
(3)工业上电解Na2CO3溶液可以生成NaHCO3和NaOH两种工业重要原料,装置如图所示。
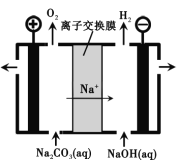
①电解的总反应式___________________________。
②已知H2CO3的Ka1=4.30×10-7, Ka2=5.60×10-11, 当同浓度的稀NaHCO3和稀Na2CO3溶液以2∶1体积比混合后,混合液的c(H+)约为____________ mol·L-1。
(4)为测定某NaNO2 溶液的物质的量浓度, 准确量取10.00mLNaNO2 溶液样品与24.00mL 0.05000mol·L-1 过量的酸性KMnO4 溶液充分反应,反应后所得溶液用0.1000mol/L(NH4)2Fe(SO4)2 标准溶液滴定至终点,消耗(NH4)2Fe(SO4)2 溶液 10.00mL。 终点的现象_____________________,通过计算确定NaNO2 溶液的物质的量浓度___________ mol·L-1。
有关反应式:5NO2-+2MnO4-+6H+=5NO3-+2Mn2++3H2O; 5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施是为了减慢化学反应速率的是
A.合成氨工业中使用催化剂
B.用铁粉代替铁钉与稀硫酸反应制取氢气
C.食品放在冰箱中贮藏
D.在试管中进行铝和盐酸反应时,稍微加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温常压下能大量共存,并可用浓硫酸干燥的一组气体是( )
A.SO2、HI、N2B.O2、CO2、NO
C.NH3、N2、H2D.O2、H2、SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于铁及其化合物的叙述正确的是( )
A.铁是一种较活泼的金属
B.Fe2O3在常温下可以导电
C.Fe2O3溶于水生成Fe(OH)3
D.在常温下铁丝容易与水反应放出H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种由菱镁矿(主要成分MgCO3、CaCO3、FeCO3、SiO2)制备高纯氢氧化镁的工艺如下:
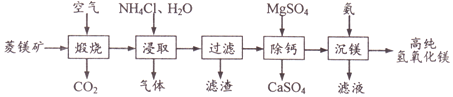
(1)“煅烧”时FeCO3发生反应的方程式为_____。
(2)“浸取”温度100℃左右,该步骤含镁化合物参与反应的化学方程式为______。
(3)“浸取”时NH4Cl用量对Mg2+浸出率的影响曲线如右图所示。下列有关说法正确的____(填序号)。

A.“浸取”时适当搅拌浆料
B.用超理论用量20%的NH4Cl进行浸取
C.可用NH4Cl对浸取后的滤渣进行二次浸取,将两次浸取液合并
D.浸出温度采用100℃可促进NH4Cl的水解和NH3的逸出
(4)本工艺流程中可循环利用的物质有______。
(5)若要得到高纯Mg(OH)2,需对“沉镁”步骤所得的固体进行洗涤,检验固体已洗净的方法是_______。
(6)25℃时,Ksp(CaSO4)=7.2×10-5。实验测得“除钙”前后溶液中c(Ca2+)分别为2.8g/L和0.8g/L,则1L溶液至少需加入MgSO4固体的质量为____g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方法能使体系中水的电离平衡逆向移动的是( )
A. 加热Na2SO4溶液
B. CH3COONH4 不饱和溶液中加入少量CH3COONH4固体
C. 水中加入少量金属 Na
D. Na2CO3溶液中加入少量BaCl2固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下图所示实验装置(夹持仪器己略去)探究铜丝与过量浓硫酸的反应。下列实验不合理的是( )
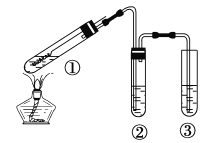
A. ②中选用品红溶液验证SO2的生成
B. ③中选用NaOH溶液吸收多余的SO2
C. 为确认有CuSO4生成,向①中加水,观察颜色
D. 上下移动①中铜丝可控制SO2的产生与停止
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】世界卫生组织(WHO)将ClO2 列为A级高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有广泛的应用.ClO2属于( )
A.酸
B.碱
C.氯化物
D.氧化物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com