
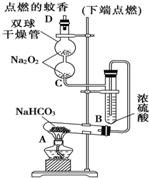
 如图实验装置用于验证某些物质的性质.在试管A中装入足量的固体NaHCO3,D为固定有燃着蚊香的硬纸片.试回答下列问题:
如图实验装置用于验证某些物质的性质.在试管A中装入足量的固体NaHCO3,D为固定有燃着蚊香的硬纸片.试回答下列问题:分析 加热A试管,发生2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,B中浓硫酸起到干燥的作用,二氧化碳再C中与过氧化钠反应生成氧气,可使D中燃着蚊香燃烧更加剧烈,说明过氧化钠和二氧化碳反应生成氧气,如将干燥管内的Na2O2换成Na2O,则不生成氧气,蚊香逐渐熄灭,以此解答该题.
解答 解:(1)加热碳酸氢钠固体的反应生成碳酸钠和二氧化碳水,反应的化学方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,
故答案为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
(2)B中盛的是浓硫酸起到吸收水蒸气干燥二氧化碳气体,故答案为:吸收气体中的水蒸气(干燥CO2);
(3)过氧化钠和二氧化碳反应生成碳酸钠和氧气,反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2,
故答案为:2Na2O2+2CO2=2Na2CO3+O2↑;
(4)氧化钠是淡黄色固体,随反应进行变为白色固体碳酸钠,反应生成氧气具有助燃性,蚊香燃烧更剧烈,
故答案为:淡黄色的Na2O2逐渐转变为白色粉末,点燃的蚊香燃烧更加剧烈;
(5)氧化钠和二氧化碳反应生成碳酸钠,无氧气生成,在二氧化碳环境,蚊香逐渐熄灭.
故答案为:点燃的蚊香逐渐熄灭.
点评 本题考查了实验装置的性质实验,为高频考点,侧重于学生的分析、实验能力的考查,装置的作用分析,反应产物的判断,物质性质和反应现象判断是解题关键.题目难度中等.


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:选择题
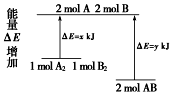
| A. | 该反应的反应热△H=x-y kJ/mol | |
| B. | 断裂1 mol A-A键和1 mol B-B键放出x kJ能量 | |
| C. | 2 mol AB的总能量高于1 mol A2和1 mol B2总能量 | |
| D. | 该反应是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 固体中一定不含有CuSO4、FeCl3 | |
| B. | 固体中一定不含有Na2CO3、一定含有Na2SO4 | |
| C. | 固体中一定含有FeCl2,不一定含有NaCl | |
| D. | 要检验固体中有没有MgCl2,需再取一份溶液,滴加NaOH溶液,若产生白色沉淀,则含有MgCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化锰和浓盐酸共热制氯气 | B. | 煅烧黄铁矿(FeS2)制SO2 | ||
| C. | 氯气与石灰乳反应制漂白粉 | D. | 电解熔融氯化镁制金属镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
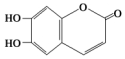 ,下列叙述正确的是( )
,下列叙述正确的是( )| A. | M的分子式为C9H6O4 | |
| B. | 1 mol M最多能与2 mol Br2发生反应 | |
| C. | 1 molM最多能与4 mol氢氧化钠反应 | |
| D. | M既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O(l)?H+(aq)+OH-(aq)△H<0 | |
| B. | 纯液态水中,一定存在Kw=[H+][OH-] | |
| C. | 纯液态水中,一定存在[H+][OH-]=1×10-14mol2•L-2 | |
| D. | 25℃,[H+]=1×10-7mol•L-1的液体一定是纯水 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含碳质量分数最大的有机物 | |
| B. | 最简单的有机物 | |
| C. | 是天然气的主要成分 | |
| D. | 与氯气在光照条件下能发生取代反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com