


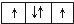


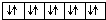
分析 (1)泡利不相容原理:每个原子轨道上最多只能容纳2个自旋状态相反的电子;
洪特规则:在同一个电子亚层中排布的电子,总是尽先占据不同的轨道,且自旋方向相同;
(2)同一元素的原子中,基态和激发态原子的核外电子总数相等,根据构造原理书写其基态原子核外电子排布式;在主族元素中,元素的最高化合价等于其族序数,从而确定其最高价氧化物对应的水化物;
(3)①同一周期中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第IIA族元素大于相邻元素,同一主族元素中,元素的第一电离能随着原子序数的增大而减小;
②同一周期中,元素的电负性随着原子序数的增大而增大,同一主族中,元素的电负性随着原子序数的增大而减小;
③电子的能层越大其能量越高,同一能层的电子,按s、p、d、能量逐渐增大.
解答 解:(1)泡利不相容原理:每个原子轨道上最多只能容纳2个自旋状态相反的电子;
洪特规则是指在同一个电子亚层中排布的电子,总是尽先占据不同的轨道,且自旋方向相同;
所以违反泡利不相容原理的有A,违反洪特规则的有 BDE,
故答案为:A;BDE;
(2)根据激发态原子核外电子排布式知该元素核外有16个电子,根据构造原理知,其基态原子核外电子排布式为:1s22s22p63s23p4,该元素是S元素,S元素最外层有6个电子,其最高化合价是+6价,其最高价氧化物对应的水化物是硫酸,其化学式为H2SO4,
故答案为:1s22s22p63s23p4;H2SO4;
(3)①同一周期中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第IIA族元素大于相邻元素,同一主族元素中,元素的第一电离能随着原子序数的增大而减小,所以第一电离能:Na<Mg,Mg>Ca,
故答案为:<;>;
②同一周期中,元素的电负性随着原子序数的增大而增大,同一主族中,元素的电负性随着原子序数的增大而减小,所以电负性:O<F,F>Cl,
故答案为:<;>;
③电子的能层越大其能量越高,同一能层的电子,按s、p、d、能量逐渐增大,所以能量高低:ns<(n+1)s,ns<np,
故答案为:<;<.
点评 本题考查了原子核外电子排布、元素周期律等知识点,根据泡利原理、洪特规则、元素周期律来分析解答,易错点是第一电离能的异常现象,当原子轨道处于半满、全满、全空时原子最稳定,难度中等.


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:解答题
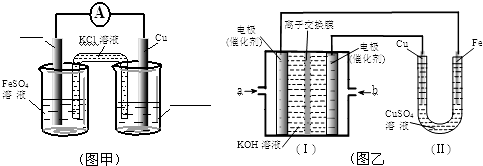
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
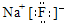 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
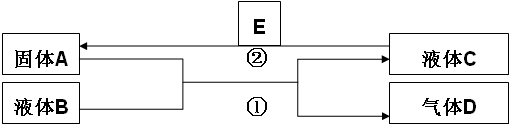
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化碳的结构式:O-C-O | |
| B. | 氢氧根离子的电子式: | |
| C. | 四氯化碳的电子式: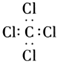 | |
| D. | 用电子式表示氯化氢分子的形成过程: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
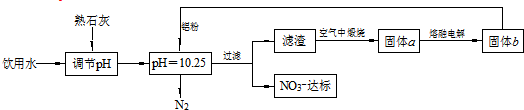
| A. | 该方案在调节pH时,若pH过大或过小都会造成Al的利用率降低 | |
| B. | 在加入铝粉的反应中,氧化产物和还原产物的物质的量之比为10:3 | |
| C. | 用熟石灰调节PH主要原因是价格便宜且引入的Ca2+对人体无毒 | |
| D. | 为了降低能耗,工业上往往用AlCl3代替固体a来制备固体b |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com